
На этой странице вы узнаете
- Насколько от размера углеводорода зависит его токсичность?
- Как связаны циклоалканы и нефть?
- Не имей сто рублей, а имей сто производных — где находят применение производные циклогексена?
Циклические соединения — соединения, уникальные как по своим химическим свойствам, так и по своему строению. Какую роль циклоалканы и циклоалкены играют в промышленности, на кого они больше всего похожи и что такое «банановая связь» — ответы на эти и другие вопросы мы узнаем сегодня.
Общая характеристика циклоалканов и циклоалкенов
Для начала нам стоит понять, что же из себя представляют циклические соединения, а для этого дадим им определения.
Циклоалканы — предельные циклические углеводороды, состав которых выражается общей формулой CnH2n (n≥3). В молекулах циклоалканов все атомы углерода соединены одинарными связями и замкнуты в цикл.
Атомы углерода замкнуты в цикл, присутствуют только одинарные связи — перед нами циклоалкан!
Разберем подробнее строение циклоалканов:
- гибридизация атомов C: sp3;
- связи: одинарные (сигма-);
- форма молекул: молекулы объемные, имеют тетраэдрические/зигзагообразные фрагменты;
- валентный угол: различен у разных циклов.
В простейших циклах C3H6 и C4H8 углы между связями C−C сильно отличаются от тетраэдрического угла 109°28՛, что создает в молекулах напряжение, из-за которого связи лежат не вдоль оси, соединяющей ядра атомов, а отклоняются от нее, напоминая банан («банановую связь»). Данный тип связи обеспечивает высокую реакционную способность — способность вещества вступать в химические реакции. Молекула циклопропана имеет плоское строение, валентные углы между атомами углерода равны 60°.
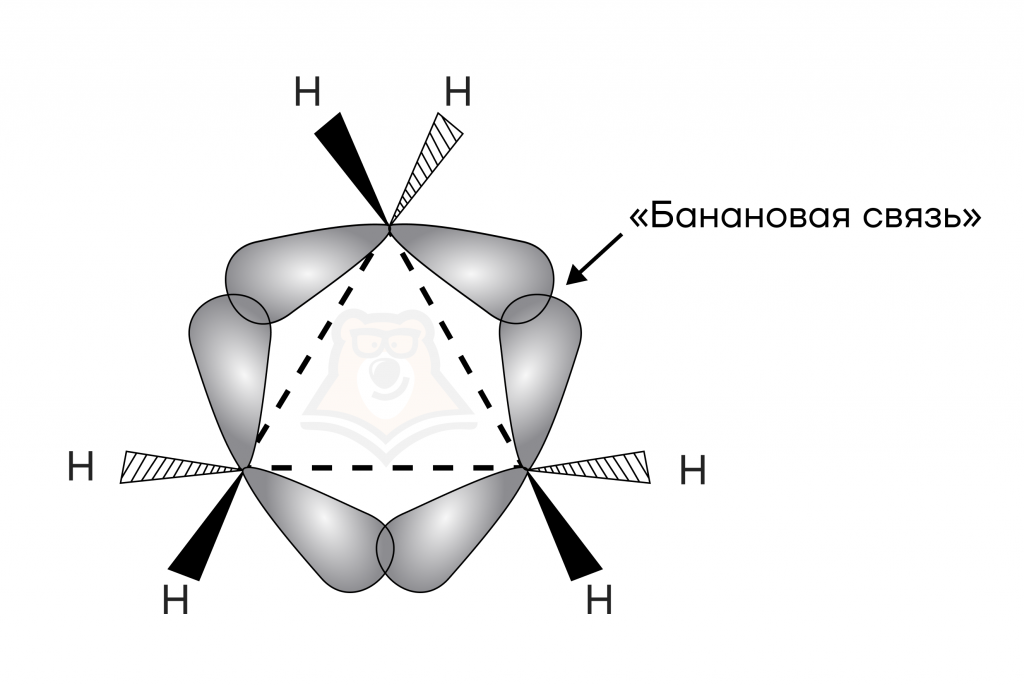
Перейдем к циклоалкенам.
Циклоалкены — непредельные циклические углеводороды, состав которых выражается общей формулой CnH2n-2 (n≥3). В молекулах циклоалкенов все атомы углерода замкнуты в цикл, при этом два атома углерода соединены кратной (двойной) связью.
Атомы углерода замкнуты в цикл, но есть одна двойная связь — это циклоалкен!
Строение циклоалкенов аналогично строению циклоалканов за исключением участка с кратной связью, в нем гибридизация атомов углерода sp2, а связи двойные (сигма и пи).
Теперь, когда мы изучили химические строение циклических соединений, закрепим наши знания на примере задания №11 ЕГЭ.
Задание. Из предложенного перечня выберите два вещества, в молекулах которых находятся атомы углерода только в sp3-гибридном состоянии.
1) циклобутен;
2) пропен;
3) циклогексан;
4) циклопентен;
5) циклопропан.
Решение. Для решения данного задания нужно вспомнить, что все вещества, содержащие кратную связь (алкены, алкины, циклоалкены) содержат также атомы углерода в sp2-гибридном состоянии.
По этому принципу мы отклоняем алкен (пропен) и циклоалкены (циклобутен и циклопентен).
Остаются только циклогексан (1) и циклопропан (5) — циклоалканы, в молекулах которых действительно все атомы углерода находятся в sp3-гибридном состоянии.
Ответ: 15
А теперь перейдем к изучению «имен» циклических соединений.
Номенклатура
Названия циклоалканов и циклоалкенов образуют путем добавления приставки «цикло-» к названию соответствующего алкана или алкена:
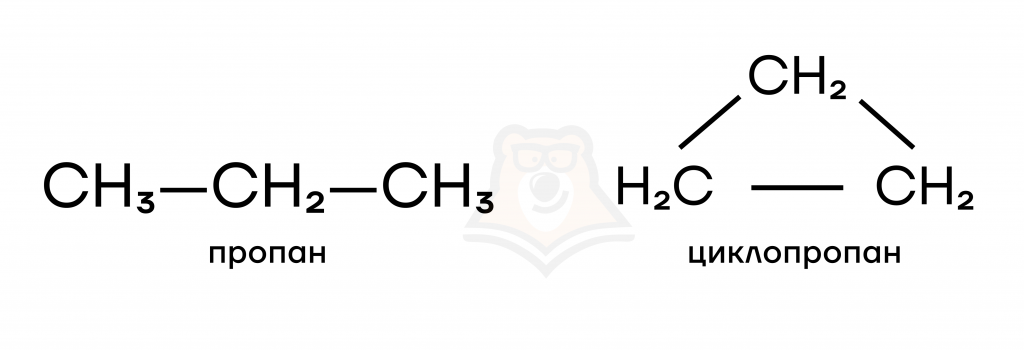
О том, как образуются названия алканов, можно прочитать в статье «Алканы», а о номенклатуре алкенов можно прочитать в статье «Алкены».
Если в циклическом соединении есть заместители (группа атомов, замещающих водород), то их нужно пронумеровать. Называем вещество по схеме: «положение и название заместителей» + «название цикла (каркаса молекулы)». Если заместителей несколько, то оперируем приставками ди-, три- или тетра-, а если заместители разные, то расставляем их по алфавитному порядку.
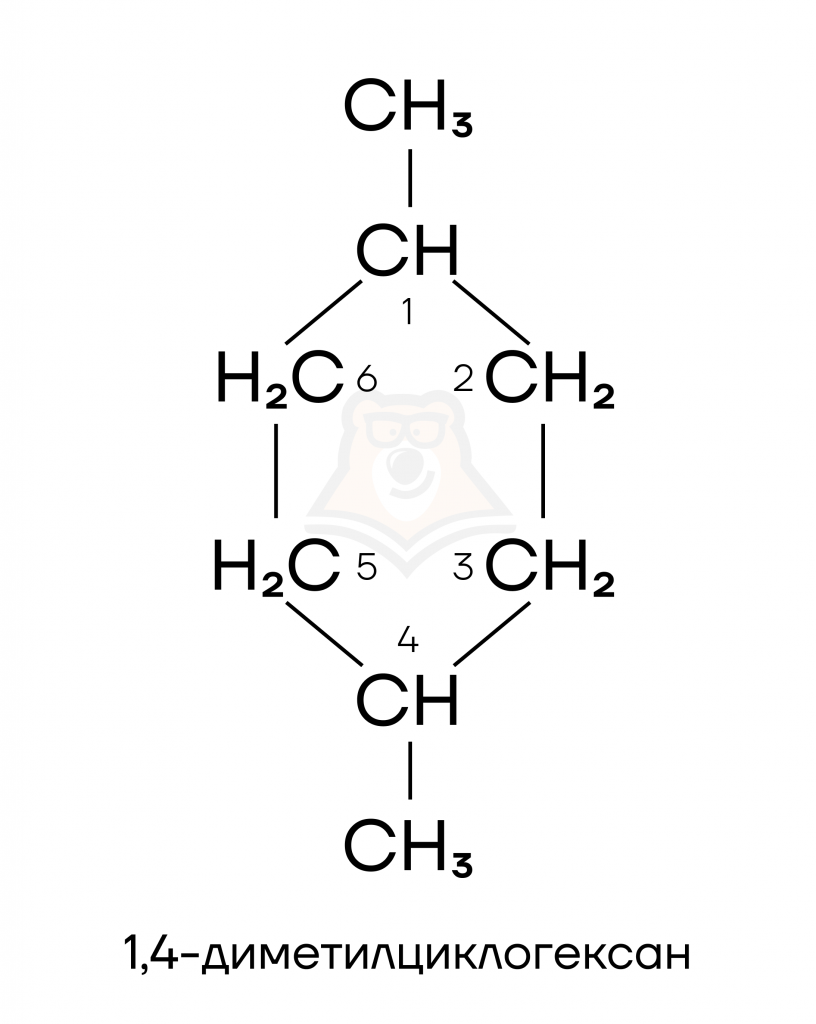
На 1 и 4 позициях два метильных заместителя, то есть радикалы у нас могут быть названы как 1,4-диметил. Добавляем название каркаса (циклогексан) и получаем 1,4-диметилциклогексан.
Разберем гомологический ряд циклических соединений и их физические свойства.
По числу атомов углерода циклы подразделяются на малые циклы (3 или 4 атома углерода) и большие (больше четырех, обычно до шести).
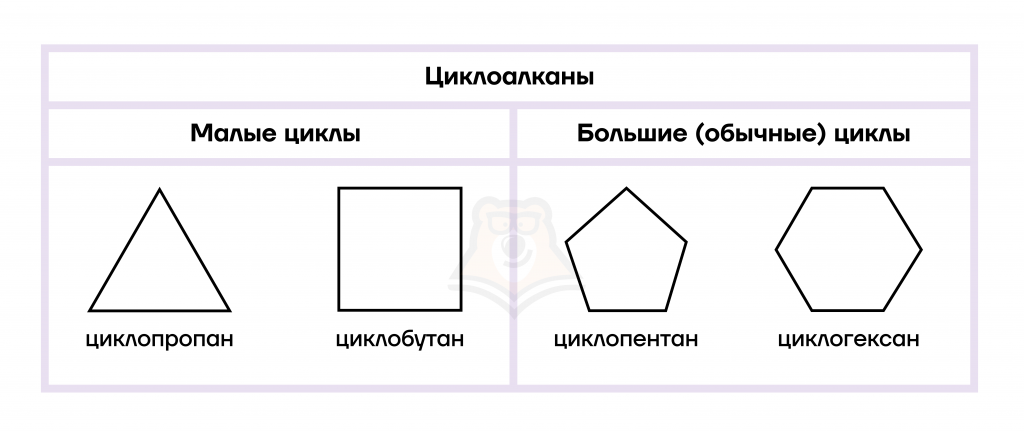
| Насколько от размера углеводорода зависит его токсичность? Циклопропан используется как средство для наркоза, циклобутан также обладает легким наркотическим действием. При дальнейшем увеличении углеродной цепи свойства циклоалканов изменяются с нейтральных на негативные: циклопентан малотоксичен, а вот циклогексан является ядовитым соединением. |
От размера цикла зависят его физические свойства: малые циклы — газы, а большие — жидкости.

Запишем также основных представителей класса циклоалкенов:
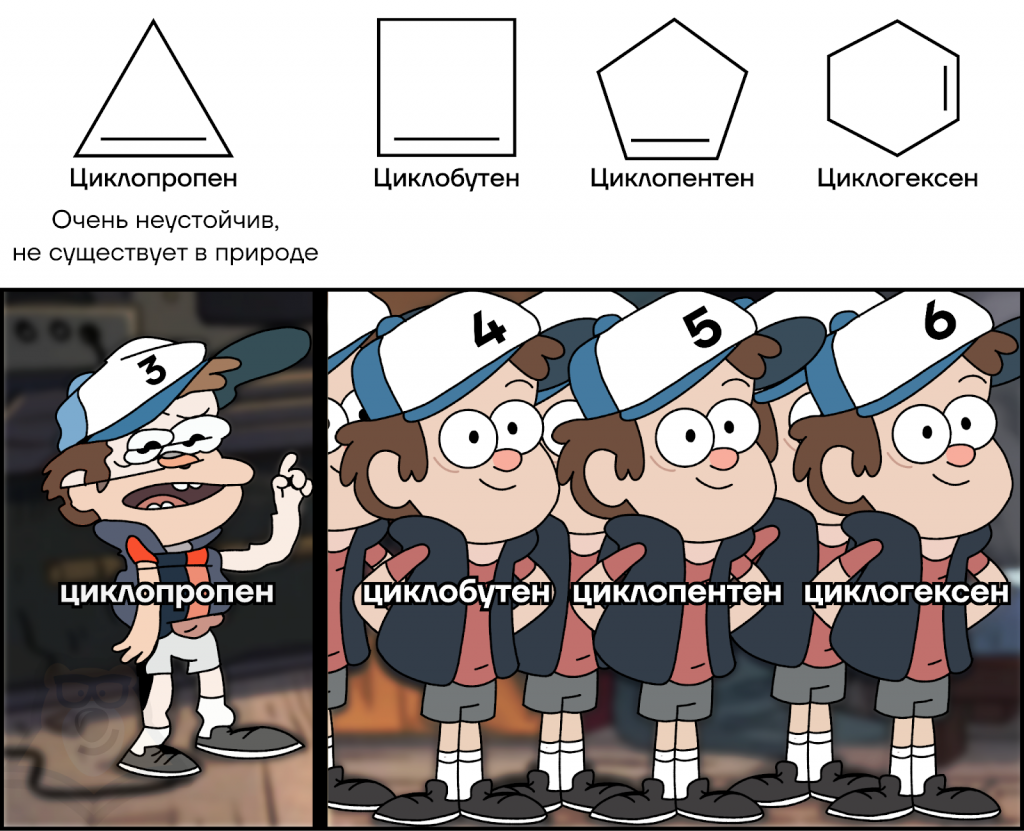
Физические свойства циклоалкенов (масса, плотность и температура кипения) зависят от их молекулярной массы, количества двойных связей, которые они имеют, и радикалов, которые к ним присоединены.
Циклоалкены плохо растворимы в воде, они растворимы в органических соединениях, и, таким образом, соблюдается принцип «подобное растворяется в подобном». Подробнее об этом принципе мы рассказывали в статье «Реакции ионного обмена».
После знакомства с циклическими соединения перейдем к знакомству с «братьями-близнецами» наших соединений.
Изомерия циклических веществ
Как для циклоалканов, так и для циклоалкенов характерна изомерия углеродного скелета.
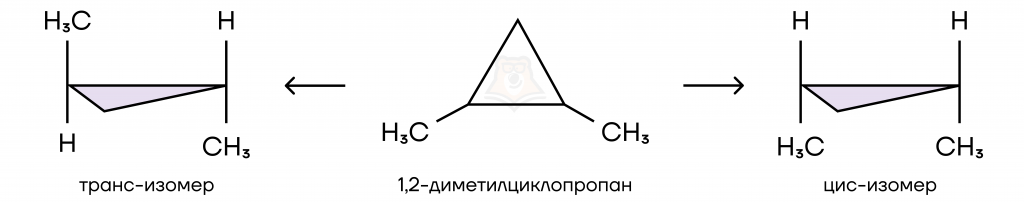
Также характерна геометрическая (пространственная) изомерия. Данный тип изомерии связан с положением в пространстве заместителей относительно плоскости цикла. Соединения, в которых одинаковые заместители располагаются по одну сторону от плоскости цикла — цис-изомеры. А те соединения, в которых одинаковые заместители располагаются по разные стороны от плоскости цикла — транс-изомеры.

Для существования цис-транс-изомеров необходимо наличие двух или более радикалов у различных атомов углерода, при этом радикалы у одного атома углерода должны быть различны.
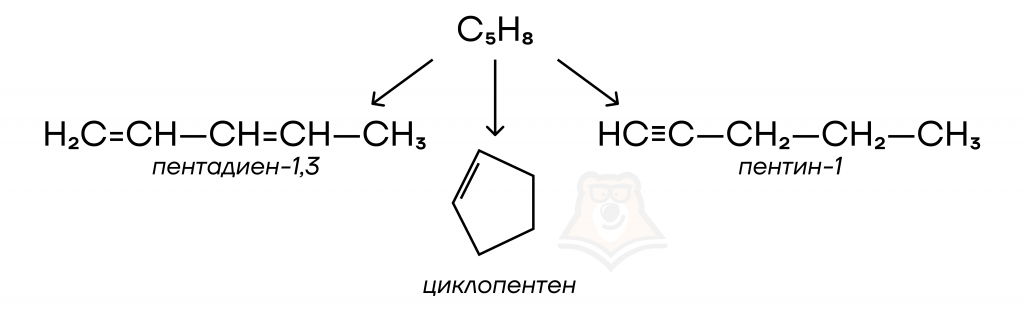
Обоим классам веществ характерна межклассовая изомерия — изомерия, при которой изомеры относятся к разным классам: изомерами циклоалканов являются алкены, а изомерами циклоалкенов — алкины и алкадиены.
Настало время узнать, каким образом могут быть получены данные соединения.
Способы получения
Циклические вещества имеют огромное значение в промышленности, поэтому так важно изучить их способы получения и применение. К основным способам получения циклоалканов относятся.
- Гидрирование аренов, в ходе которого к ароматическим соединениям добавляется водород.
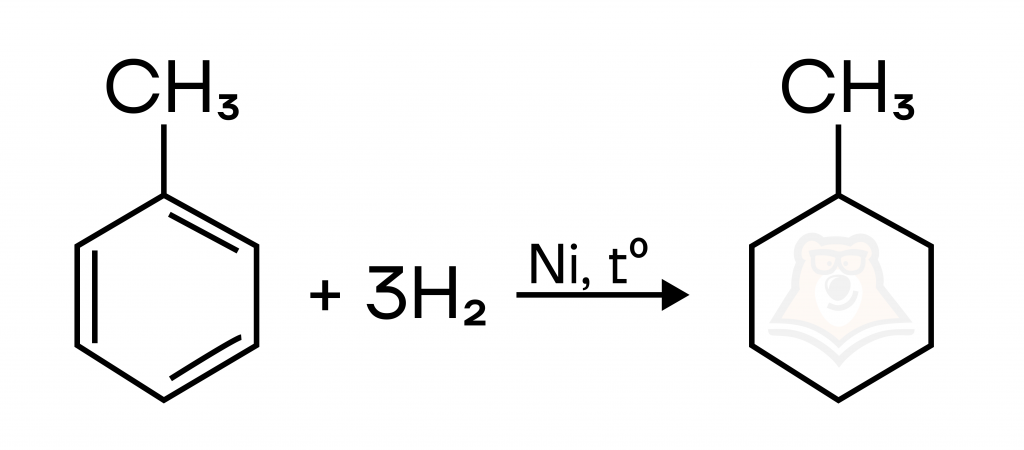
- Дегидроциклизация алканов, в ходе которого от алканов отщепляется водород, а углеродная цепочка замыкается в цикл.
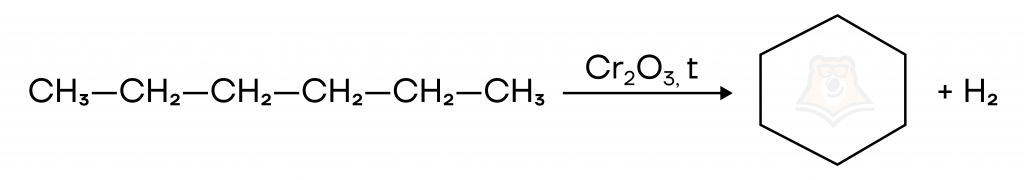
- Дегалогенирование дигалогенпроизводных с использованием Zn или Mg, при этом между атомами галогенов должно быть 3 или более атомов углеродов:
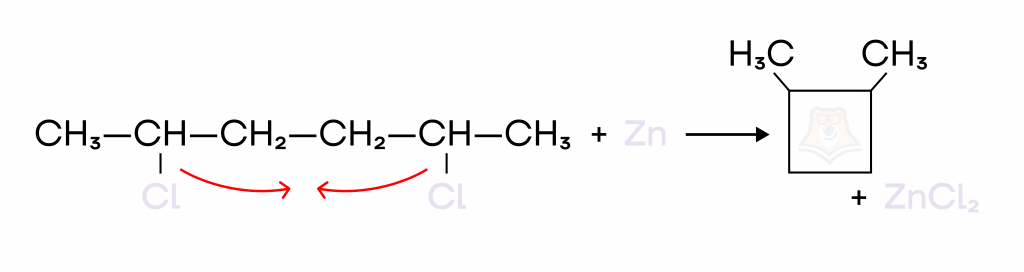
| Как связаны циклоалканы и нефть? Циклоалканы могут быть получены из нефти, но это не единственная точка пересечения этих двух веществ. Циклоалканы также применяются как добавка к бензинам (C5H10), улучшающая качество топлива. Циклоалканы могут применяться и в других сферах, например, как реагенты в получении аренов, растворители (C6H12) и реагенты в процессе синтеза синтетических волокон (C6H12). |
Способы получения циклоалкенов аналогичны способам получения алкенов.
- Дегалогенирование дигалогенпроизводных с использованием Zn или Mg, при этом между атомами галогенов должно быть 2 атома углерода.
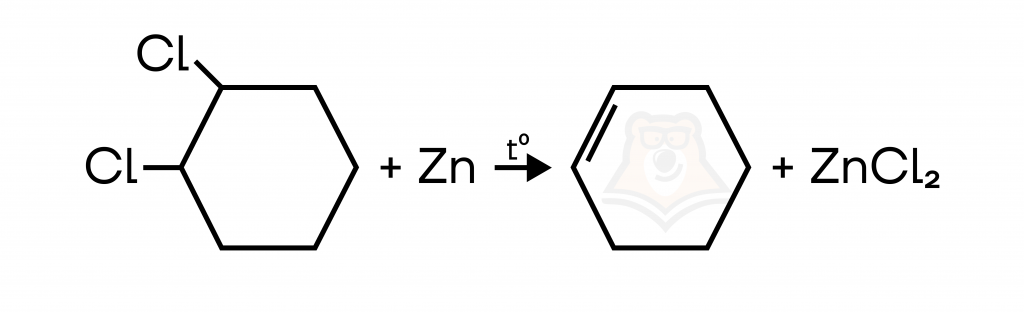
- Дегидратация спиртов при температуре выше 140℃ в присутствии серной кислоты (или иного водоотнимающего соединения вроде H3PO4, захватывающего воду из продуктов реакции).
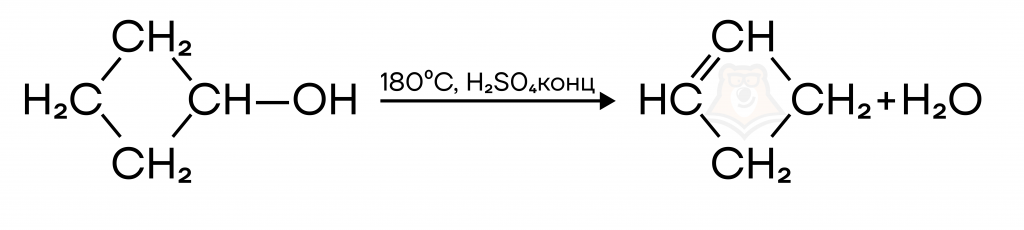
- Дегидрогалогенирование моногалогенпроизводных спиртовым раствором щелочи.
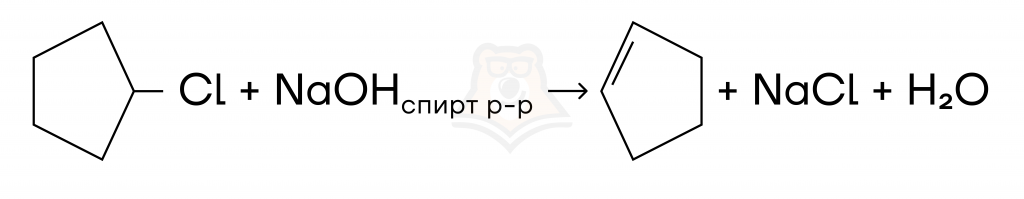
Перейдем к рассмотрению химических свойств циклических соединений.
Химические свойства
- Свойства циклоалканов
Вне зависимости от размера цикла циклоалканы вступают в реакции горения:
С6H12 + 9O2 = 6CO2 + 6H2O
В реакцию окисления при комнатных условиях циклоалканы не вступают. В жестких условиях циклоалканы могут окислиться до дикарбоновой кислоты, реакция протекает с разрывом связи внутри цикла. Практическое значение имеет окисление циклогексана.
Реакции окисления циклоалканов не встречаются на экзамене.
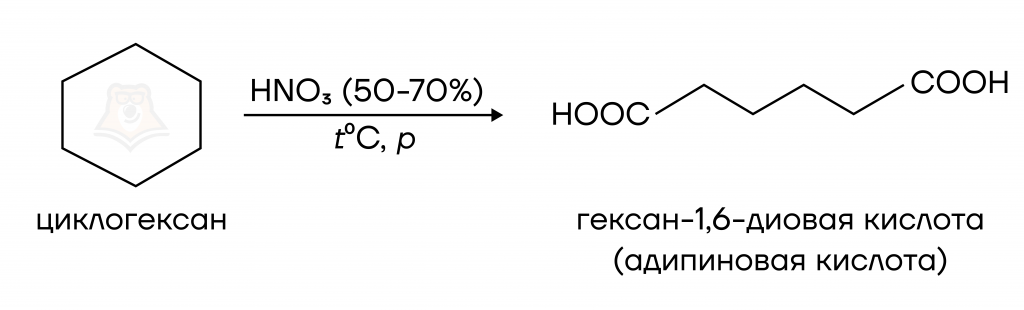
Остальные химические свойства зависят от размера цикла.
- Свойства малых циклов
Малые циклы вступают в реакции присоединения (галогенирования, гидрирования или гидрогалогенирования), которые сопровождаются разрывом цикла:
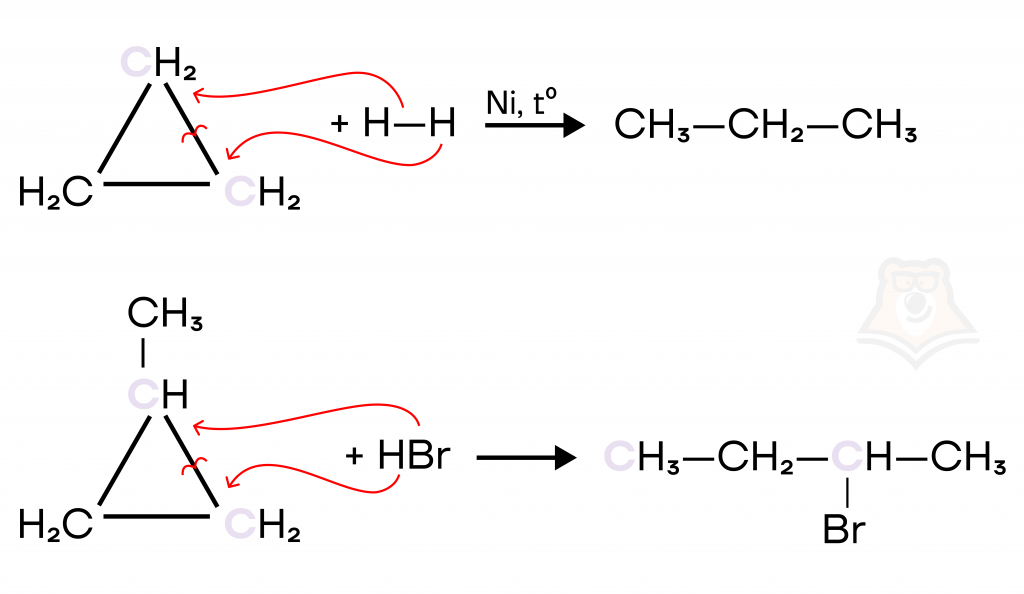
- Свойства больших циклов
Большие циклы вместо реакций присоединения вступают в реакции замещения (галогенирование, нитрование, сульфирование), при которых разрыва цикла не происходит:
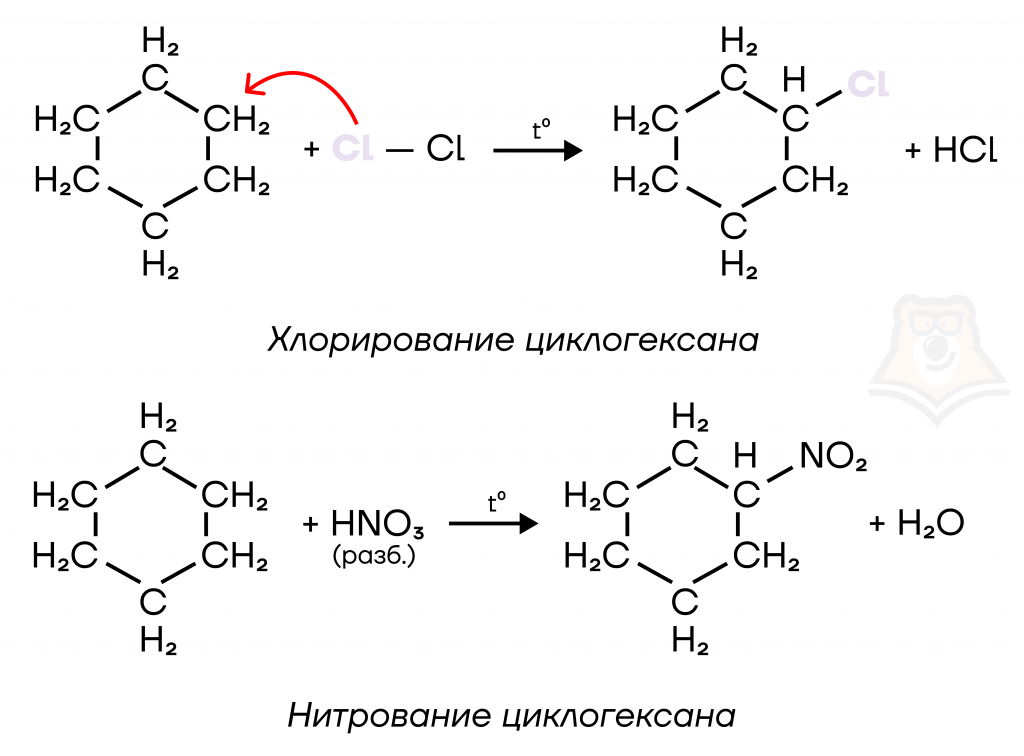
В жестких условиях (при высокой температуре) в реакцию присоединения вступает циклопентан, хотя не относится к малым циклам:
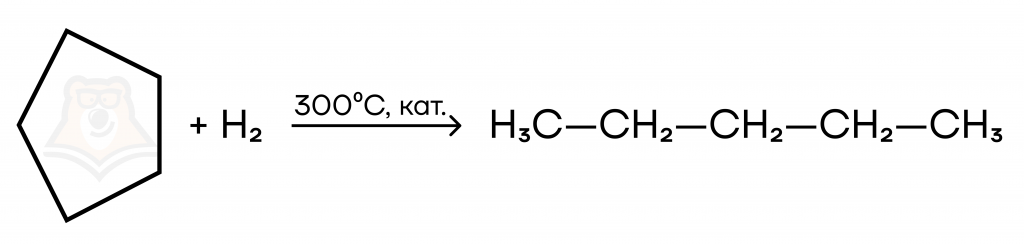
Большие циклы также вступают в реакции дегидрирования с образованием циклоалкенов или вступают в реакцию ароматизации — дегидрирование с получением бензола:
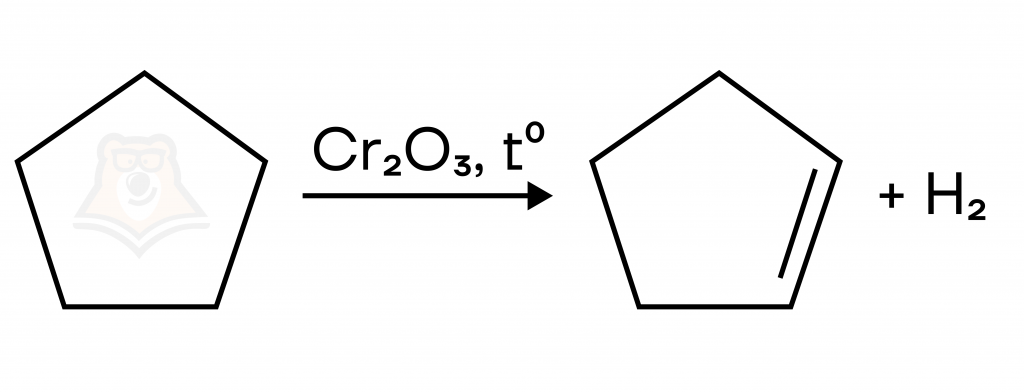
Дегидрирование циклопентана с образованием циклопентена
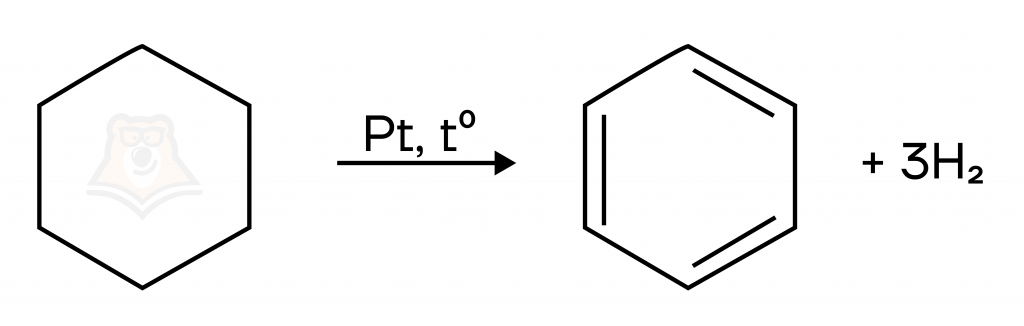
Ароматизация циклогексана
Подведем итог, какие же химические свойства характерны циклоалканам:
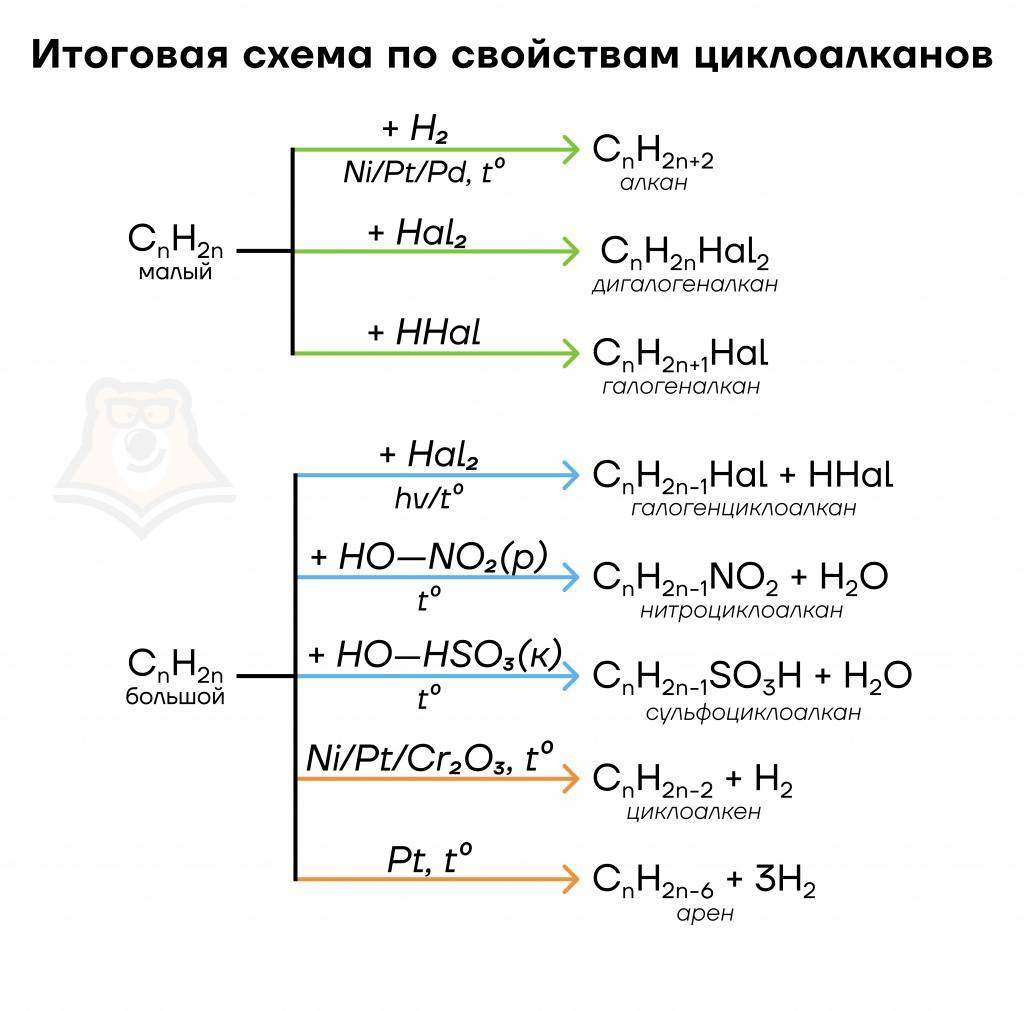
А для лучшего усвоения полученных знаний, решим аналог задания №12 ЕГЭ.
Задание. Из предложенного перечня выберите все вещества, которые могут реагировать с циклопропаном.
1) вода;
2) водород;
3) азотная кислота;
4) соляная кислота;
5) серная кислота.
Решение. Вспомним, что для малых циклов характерны реакция присоединения: гидрирование, галогенирование и гидрогалогенирование. Таким образом, возможно протекание реакции с водородом и соляной кислотой.
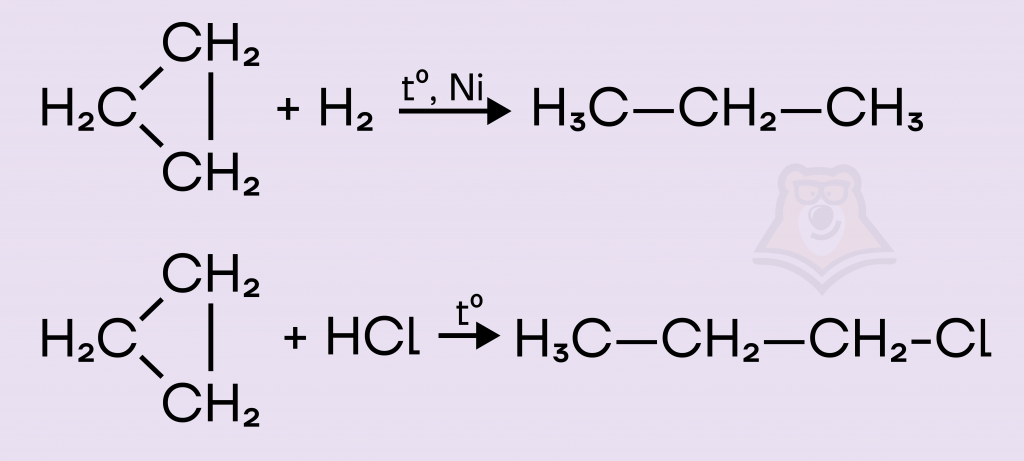
С азотной и серной кислотами реагируют только большие циклы, поэтому данные варианты ответа мы отметаем.
Взаимодействие с водой для циклоалканов невозможно.
Ответ: 24
На этом химические свойства циклоалканов заканчиваются, перейдем к свойствам других циклических соединений — циклоалкенов.
- Свойства циклоалкенов
Циклоалкены похожи на алкены, свойства которых мы рассматривали в статье «Алкены».
Аналогично алкенам, циклоалкены вступают в реакции присоединения и окисления.
Присоединять циклоалкены могут галогены, галогеноводороды, воду и сам водород.
Присоединение бромной воды является качественной реакцией на двойную связь, оранжевый раствор бромной воды обесцвечивается.
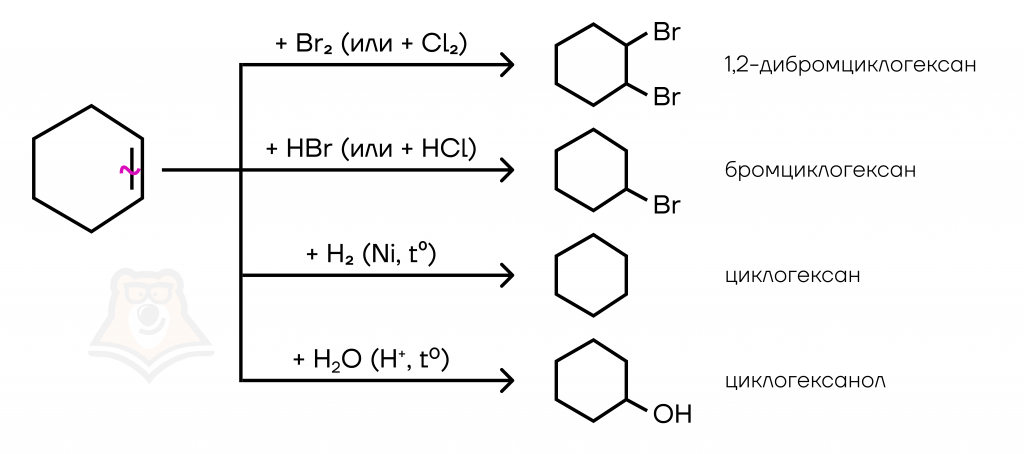
Реакции окисления циклоалкенов можно разделить на мягкое и жесткое окисление.
В ходе мягкого окисления в нейтральной среде без нагревания образуется диол. Реакция является качественной: фиолетовый раствор перманганата обесцвечивается и выпадает бурый осадок диоксида марганца.
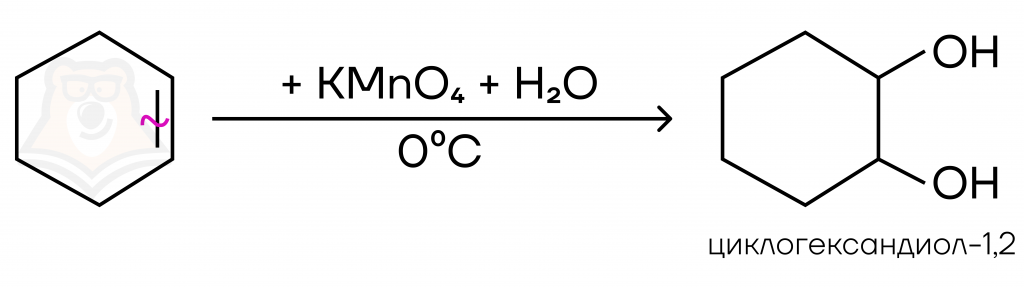
В ходе жесткого окисления, протекающего при более высоких температурах или в кислых/щелочных средах, происходит разрыв связей с образованием карбоновой кислоты или ее солей. Реакция также является качественной — наблюдается обесцвечивание раствора перманганата.
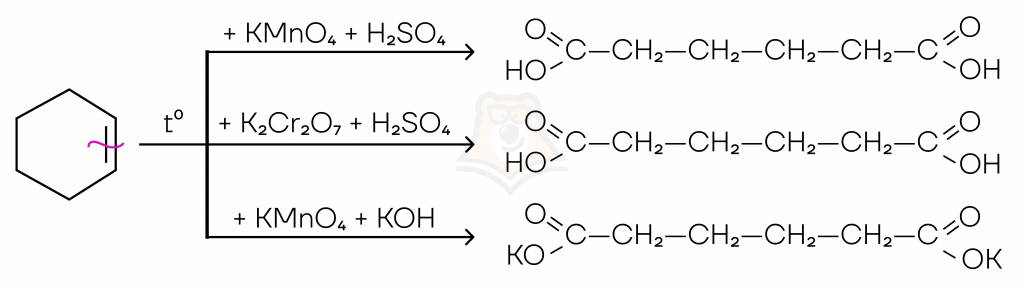
| Не имей сто рублей, а имей сто производных — где находят применение производные циклогексена? Сами циклоалкены не часто находят себе применение, но вот их производные необходимы во многих отраслях промышленности. Так, например, сам циклогексен используется как растворитель, а также как сырье для производства различных карбоновых кислот. Зато производные циклогексена имеют множество применений. — Хлорид циклогексана используется в качестве промежуточного продукта при производстве фармацевтических продуктов. — Циклогексанон является сырьем для производства лекарств, пестицидов, парфюмерии и красителей. — Циклогексен участвует в синтезе аминоциклогексанола — соединения, которое используется в качестве поверхностно-активного вещества, применяемого при производстве мыла. — Также циклогексен — это сырье для синтеза лизина, фенола, полициклоолефиновой смолы и резиновых добавок. |
Циклические соединения похожи своей цикличностью на другой класс соединений — ароматические соединения. Об основном представителе данного класса, бензоле, можно прочитать в статье «Арены. Бензол как представитель ароматических углеводородов».
Термины
Гибридизация — изменение формы и энергии электронных орбиталей разных типов.
Гомологический ряд — ряд химических соединений одного класса, отличающихся друг от друга на одну или несколько повторяющихся структурных единиц — гомологическую разность -СН2-.
Изомерия — явление, заключающееся в существовании химических соединений, одинаковых по атомному составу и молекулярной массе, но различающихся по строению.
Фактчек
- Циклические соединения включают в себя циклоалканы, в строении которых присутствуют только одинарные связи, и циклоалкены, в строении которых есть одна кратная связь.
- Название циклических соединений образуется путем прибавления приставки «цикло-».
- Циклоалканы могут быть в жидком, твердом и газообразном состояниях.
- Циклоалканам и циклоалкенам характерны пространственная, межклассовая изомерия и изомерия углеродного скелета.
- К способам получения циклоалканов относится гидрирование аренов и дегалогенирование дигалогенпроизводных, циклоалкены могут быть получены в ходе реакций дегалогенирования, дегидратации и дегидрогалогенирования.
- Химические свойства циклоалканов зависят от строения: малые циклы вступают в реакции присоединения, а большие циклы — в реакции замещения.
- Циклоалкены вступают в реакции присоединения и окисления.
Проверь себя
Задание 1.
Как выглядит общая формула циклоалканов?
- CnH2n+2;
- CnH2n;
- CnH2n-2;
- CnHn.
Задание 2.
Какие связи присутствуют в циклоалкенах?
- Двойная и одинарные
- Только одинарные
- Только двойные
- Тройная и одинарные
Задание 3.
Что образуется при взаимодействии 2,4-дихлорпентаната с цинком?
- 1,2-диметилциклопропан
- Циклопентан
- Циклопентен
- Пентен-3
Задание 4.
Какой продукт образуется в ходе гидрирования циклопентана?
- Циклопентен
- Пропан и этан
- Пентан
- Реакция не протекает
Задание 5.
Что образуется в ходе мягкого окисления циклобутена?
- Бутановая кислота
- Щавелевая кислота
- Этиленгликоль
- Циклобутандиол
Ответы: 1. — 2; 2. — 1; 3. — 1; 4. — 3; 5. — 4.

 к списку статей
к списку статей




