
На этой странице вы узнаете
- Что делает холодильники холодными?
- Кто важнее — галоген или углерод?
- Для чего могут применяться галогенпроизводные углеводородов?
Мы уже встречались с галогенпроизводными при изучении практически всех углеводородов, но теперь они не просто продукты взаимодействий веществ или реактивы для различных способов получения, они главные герои нашей статьи. Сегодня мы подробно поговорим о том, как галогенпроизводные связаны с другими классами веществ и какие они имеют уникальные свойства.

Общая характеристика галогенпроизводных углеводородов
Порой все люди задумываются над тем, кто они такие и какое их место в жизни. Выйдя из тени углеводородов, галогенпроизводные тоже столкнулись с данными вопросами. Что же они из себя представляют?
Галогенпроизводные — это производные углеводородов, в молекулах которых один или несколько атомов водорода замещены атомами галогенов.
Человека определяет его профессия, место жительства, возраст и многие другие факторы.

Например, Катя — молодая девушка, студентка биологического факультета, которая живет в Москве. Мы можем указать ее возраст, пол, место жительства и род деятельности, но все эти параметры не зависят друг от друга. Она могла бы жить в Казани, но при этом она осталась бы молодой девушкой и студенткой.
В мире галогенпроизводных каждое соединение имеет свое место, и это место также определяется различными переменными.
Исходя из количества атомов галогенов в составе соединение может быть моно-, ди-, три- и т.д. галогенпроизводным. При этом атомы галогена тоже могут быть различны: могут встречаться йод-, бром-, хлор- и фторпроизводные. А исходя из строения углеродного скелета, производные подразделяются на предельные, непредельные и ароматические.
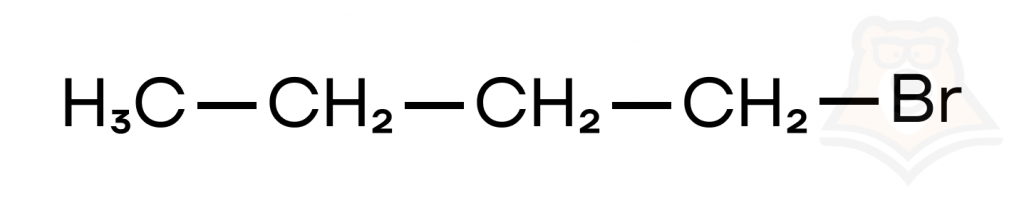
Перед нами 1-бромбутан. Это предельное монобромпроизводное бутана. Если бы мы добавили еще один атом брома, то это все еще было бы предельное бромпроизводное, но изменилась бы классификация по количеству атомов галогенов.
| Что делает холодильники холодными? Вещества, которые участвуют в процессах охлаждения, называются хладагентами. Эта большая группа веществ включает в себя фреоны — галогенсодержащие производные углеводородов. Именно фреоны используются в холодильных установках для создания и поддержания низких температур. Чаще применяются фторсодержащие соединения (например, фторметан CFH3), так как они более безопасны и экологичны: оказывают меньшее влияние на озоновый слой и усиление парникового эффекта. |
Классификация соединений также может помочь нам разобраться с названиями галогенпроизводных. Первым делом посмотрим, сколько атомов галогенов в соединении и на каком месте они располагаются. Далее остается посчитать длину углеродной цепочки и составить название по принципу «номера позиций радикалов через запятую арабскими цифрами — приставка, отражающая количество атомов галогенов + название галогена + имя углеродной цепочки». Разберемся на практике.
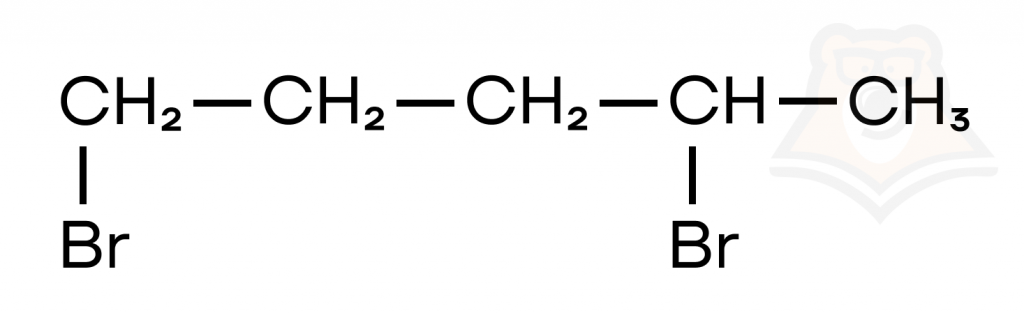
Перед нами бромпроизводное алкана. Атомы брома находятся на 1 и 4 месте, их два, значит, приставка будет ди-. В углеродной цепочке 5 атомов, перед нами пентан.
Составим название: 1,4-дибромпентан.
Если встречаются разные атомы галогенов, то названия составляются аналогично, а характеристики галогенов записываются через тире.
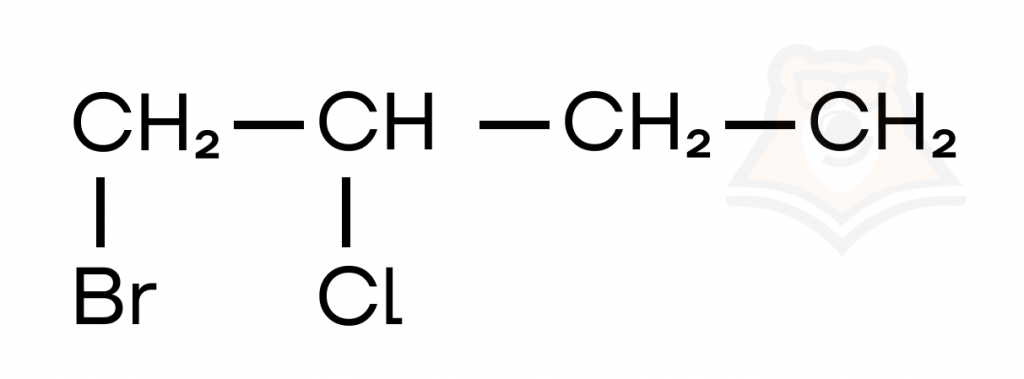
В данном соединении два различных галогена: 1 атом брома на первом месте и 1 атом хлора на втором. В углеродной цепи 4 атома, это бутан.
Составим название: 1-бром-2-хлорбутан.
| Кто важнее — галоген или углерод? Физические свойства галогеналканов зависят от длины углеродной цепочки и от количества атомов галогенов. Однако большее влияние оказывает расположение атома галогена и число данных атомов: – При переходе от первичных к вторичным и третичным галогеноалканам с одинаковым числом атомов углерода и галогена увеличиваются температуры кипения и плотность вещества. – С увеличением числа атомов галогенов возрастают температуры плавления и кипения соединения. Большинство галогеналканов являются бесцветными жидкостями, некоторые имеют сладковатый запах, но есть и кристаллические соединения, например, йодоформ СНI3. |
Строение галогенпроизводных аналогично строению соединений, от которых они образованы. Связь между атомом углерода и галогена одинарная (сигма-связь), атомы галогена не оказывают влияния на гибридизацию атомов углерода.
Для галогенпроизводных также характерна изомерия.
- Изомерия строения углеродного скелета
Суть данной изомерии заключается в изменении строения углеродной цепи путем перестановки крайних углеродов в положение радикалов или изменения положения уже имеющихся радикалов.
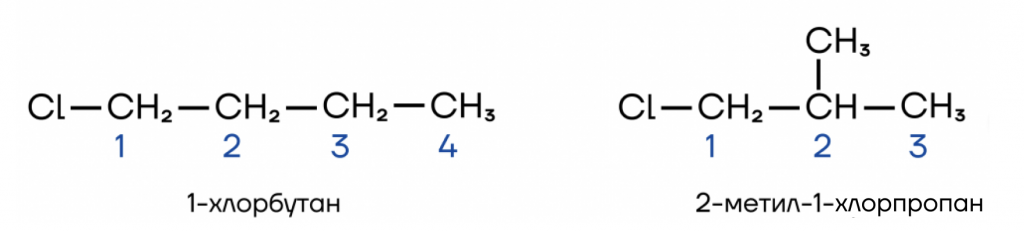
- Изомерия положения радикала
При данном типе изомерии изменяется положение радикала.
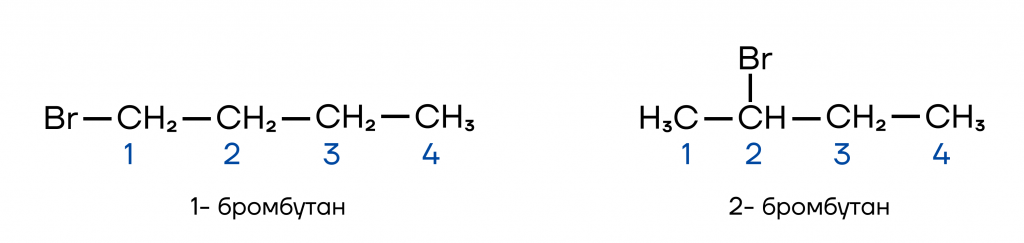
- Оптическая (пространственная) изомерия
Характерна только для производных с двойной связью или циклического строения, имеющих разные радикалы у каждого атома углерода.
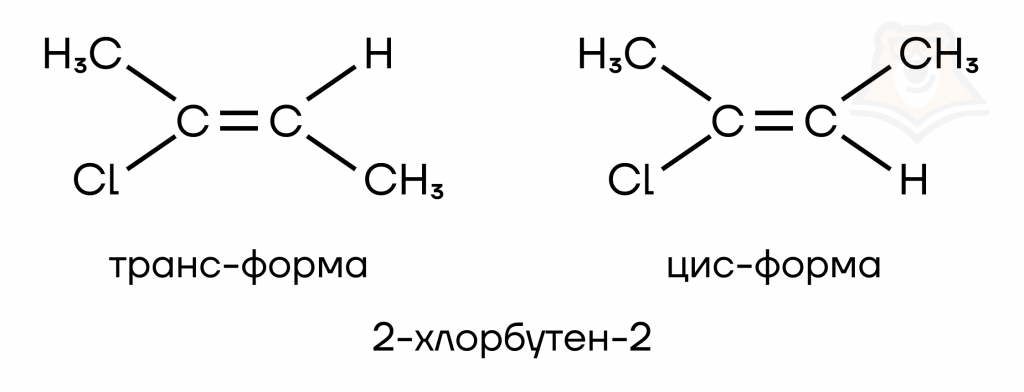
Когда основные характеристики галогенпроизводных углеводородов изучены, можем разобрать, каким же образом вещества данного класса могут быть получены.
Способы получения
Все способы получения галогенпроизводных можно разделить на несколько групп.
- Галогенирование алканов
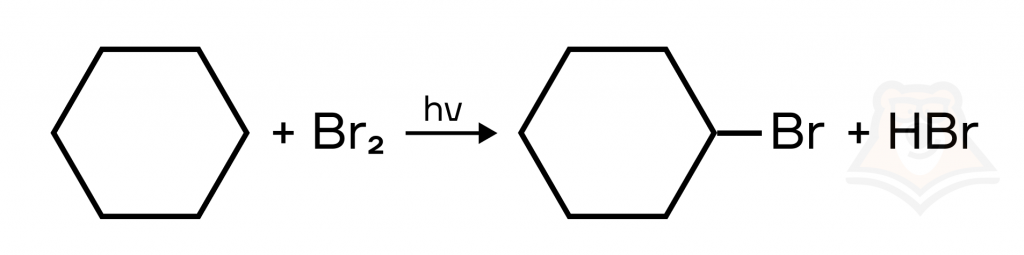
В ходе данных реакций происходит замещение атомов водорода на атом галогена с образованием галогенпроизводного и галогеноводорода. Реакция протекает на свету, за исключением взаимодействий с фтором.
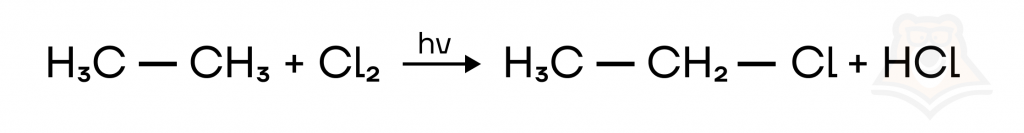
Реакции с большими циклами протекают аналогично, образуется галогенциклоалкан.
- Галогенирование непредельных углеводородов
В данной реакции происходит присоединение атомов галогена по месту кратной связи.
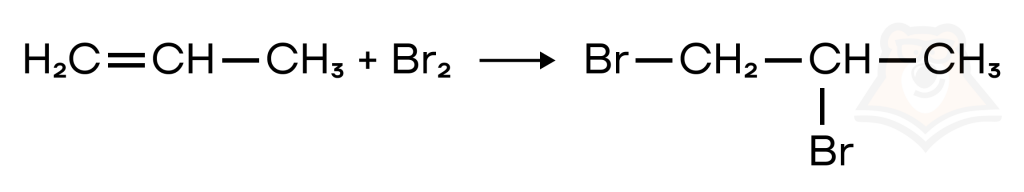
Реакции с алкадиенами, алкинами и циклоалканам протекают аналогично
- Гидрогалогенирование непредельных углеводородов
Данная реакция относится к реакциям присоединения, при взаимодействии с алкенами образуется моногалогенпроизводное, а при взаимодействии с алкинами или алкадиенами — дигалогенпроизводное.
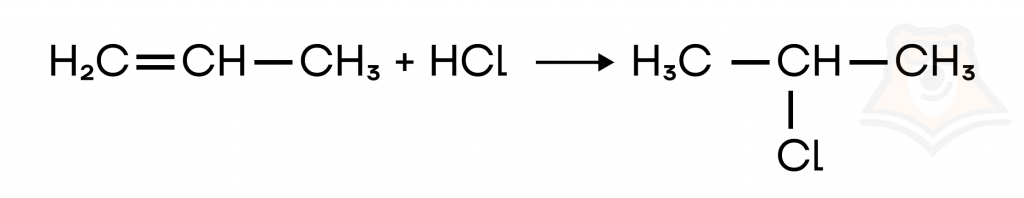
Реакция с циклоалкенами протекает аналогично
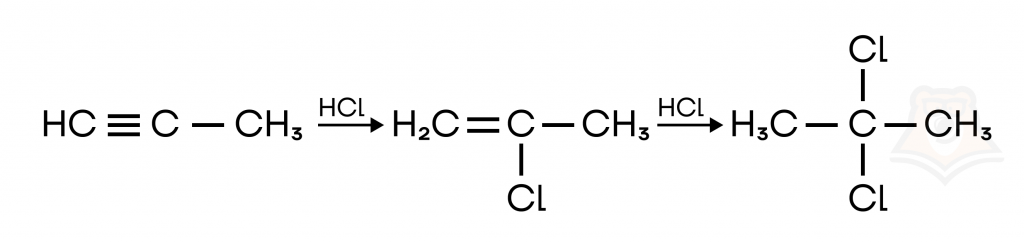
Реакция с алкадиенами протекает аналогично (в два этапа)
- Получение из спиртов
В ходе реакции происходит замещение ОН-группы на атом галогена, образуются галогенпроизводное и вода.
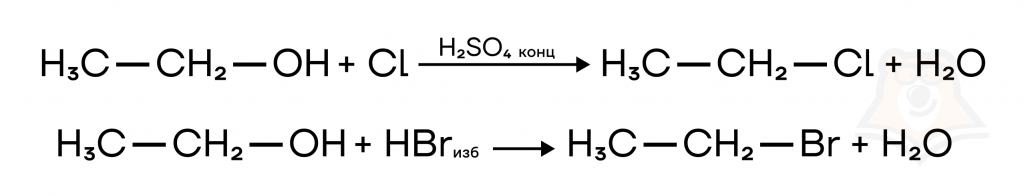
После того, как мы изучили способы получения галогенпроизводных, закрепим наши знания на примере задания №16 ЕГЭ.
Задание. Задана следующая схема превращений веществ.
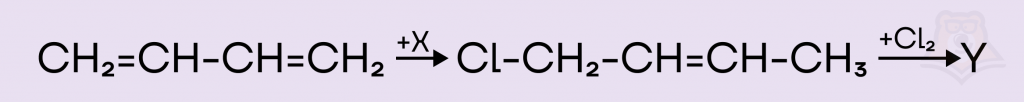
Определите, какие из указанных веществ являются веществами X и Y.
1) хлор;
2) 1,3,4-трихлорбутан;
3) 1,3,3-трихлорбутан;
4) 1,4-дихлорбутан;
5) хлороводород.
Решение. К одному из способов получения галогенпроизводных относятся реакции присоединения галогеноводородов или галогена. Так как продукт первой реакции содержит только один атом галогена, то реагентом будет хлороводород.
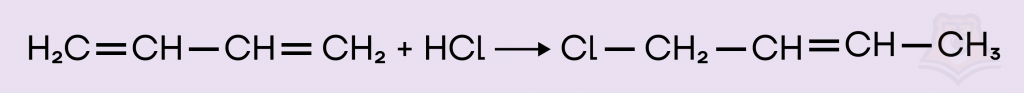
При добавлении к алкенам хлора присоединение идет к атомам, образующим кратную связь, в результате мы получаем 1,3,4-трихлорбутан.
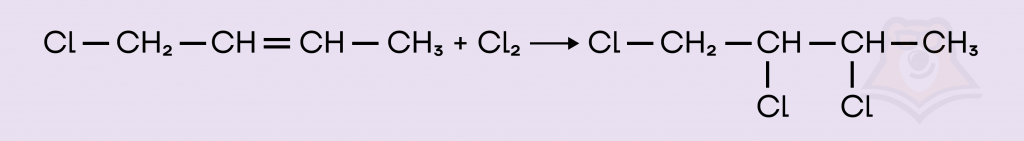
Ответ: 52
Мы уже знаем, что важнейшей характеристикой галогенпроизводных является строение, которое определяется количеством атомов углерода и галогена. Но также особенными для данного класса веществ являются химические свойства. Перейдем к ним!
Химические свойства
Разобьем все химические свойства на несколько крупных групп для удобства изучения.
- Реакции замещения
Атом галогена может быть замещен на другой галоген, ОН-, RО-, NO2-, CN-, NH2-группы. Данный тип взаимодействия относится к нуклеофильному замещению, подробную информацию о котором можно прочитать в статье «Ионный (правило В.В. Марковникова) и радикальный механизмы реакций в органической химии». Разберем некоторые реакции подробнее.
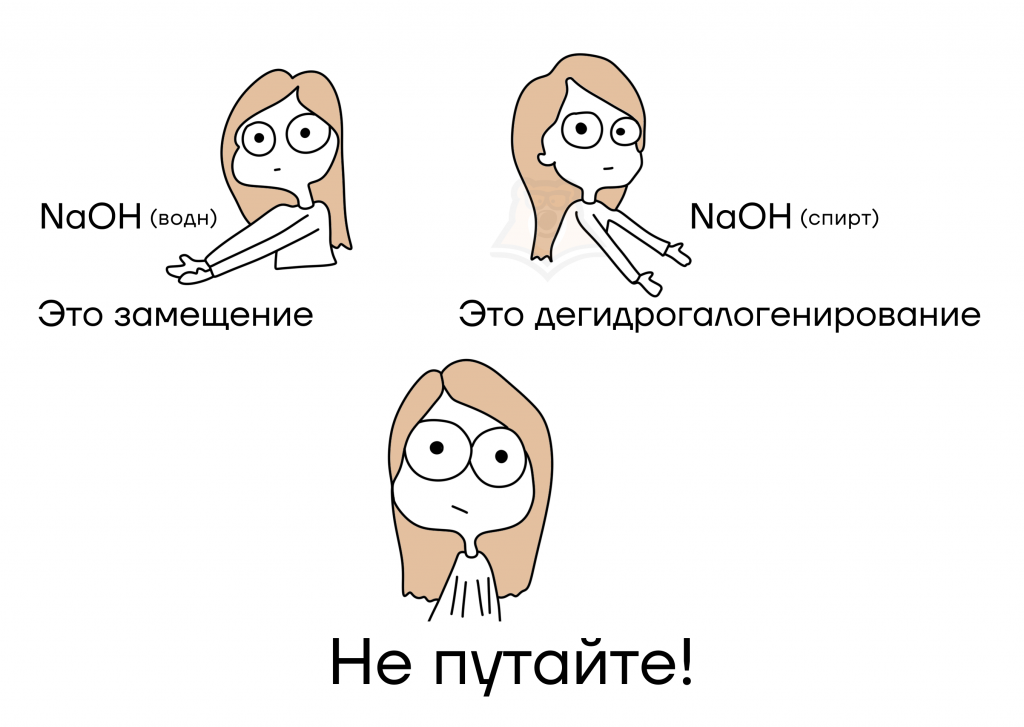
Реакция с замещением на ОН-группу протекает только с водным раствором щелочи, со спиртовым реакция иная. Также продукт реакции зависит от количества атомов галогена у одного атома углерода: при одном атоме галогена образуется спирт, при двух — кетон или альдегид (происходит отщепление одной молекулы воды), при трех — карбоновая кислота (также отщепляется молекула воды). Карбоновая кислота взаимодействует со щелочью с образованием соли, механизм данной реакции подробнее описан в статье «Карбоновые кислоты».
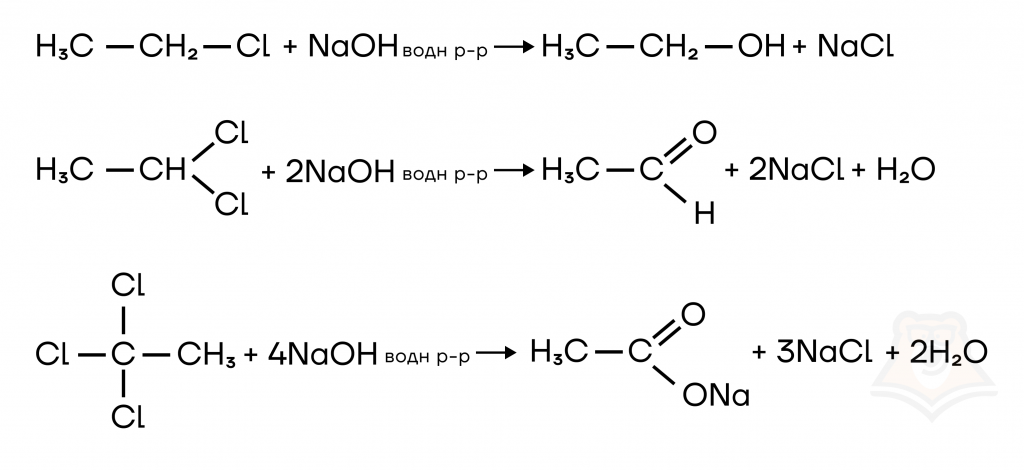
В ходе реакции замещения на NH2-группу происходит образование кислоты соответствующего галогена, что ведет к образованию соли. Подробнее о механизме в статье «Амины и аминокислоты».
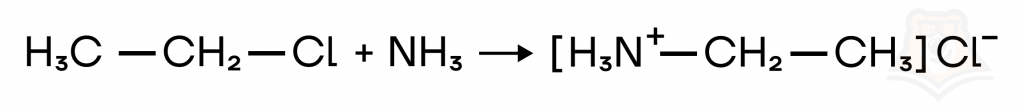
Замещение на NO2-группу происходит при присоединении нитрита серебра(I), взаимодействие протекает из-за образования неорганического осадка.
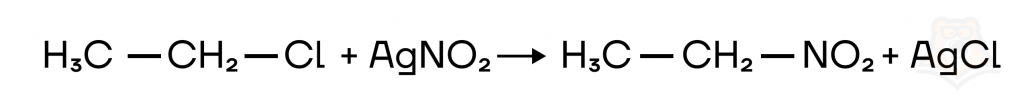
Теперь, когда мы разобрали некоторые химические свойства галогенпроизводных, решим аналог задания №12 ЕГЭ.
Задание. Из предложенного перечня выберите все вещества, с которыми хлорметан может вступать в реакции замещения.
1) аммиак;
2) спиртовой раствор щелочи;
3) водный раствор щелочи;
4) уксусная кислота;
5) нитрат серебра(I).
Решение. Атом углерода в хлорметане может быть замещен на NH2-, OH-, NO2— и некоторые другие группы.
Замещение на NH2-группу происходит при взаимодействии с аммиаком, вариант ответа под номером 1 подойдет.
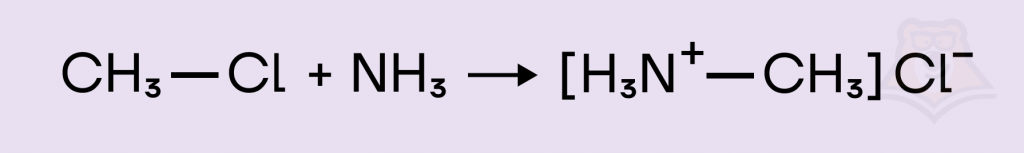
Замещение на ОН-группу протекает при взаимодействии с водным раствором щелочи, реакция со спиртовым раствором к реакциям замещения не относится. Берем в ответ вариант под цифрой 3.
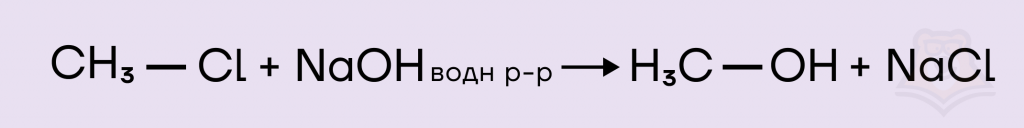
Замещение на NO2-группу протекает при реакции с нитритом, а нам дан нитрат, вариант ответа 5 не подойдет. Уксусная кислота в реакцию замещения с хлорметаном также не вступает.
Ответ: 13
- Дегидрогалогенирование
При добавлении спиртового раствора щелочи происходит отщепление галогеноводорода с образованием органического продукта, содержащего кратную связь.
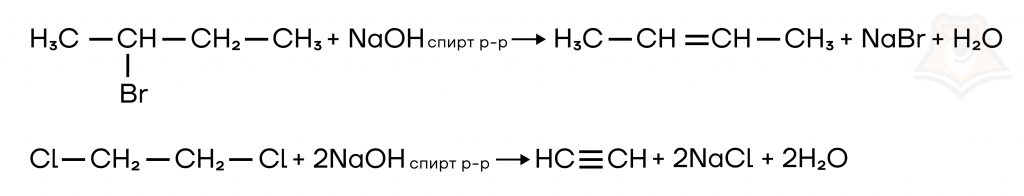
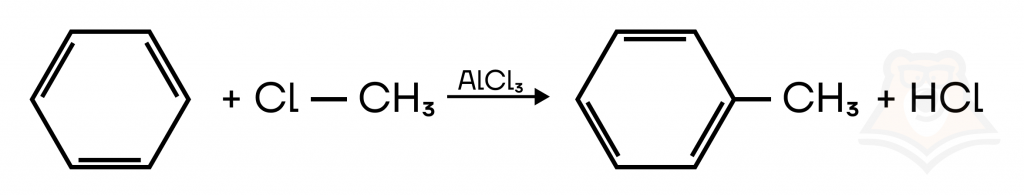
- Реакция Фриделя-Крафтса
Реакция используется для получения производных бензолов, обязательное условие реакции — катализатор AlCl3 или FeCl3.
- Реакция Вюрца
В ходе реакции происходит удваивание углеродной цепочки, образуется симметричный углеводород.
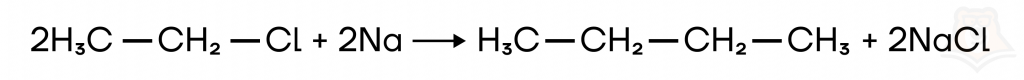
- Дегалогенирование
Протекает между дигалогенпроизводным и металлом (Zn или Mg), от положения галогенов зависят продукты.
- При соседнем расположении образуется кратная связь.
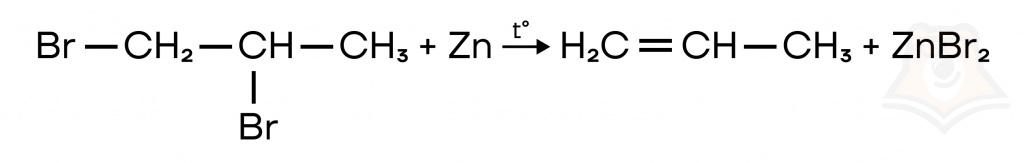
- При удаленном расположении образуется цикл.
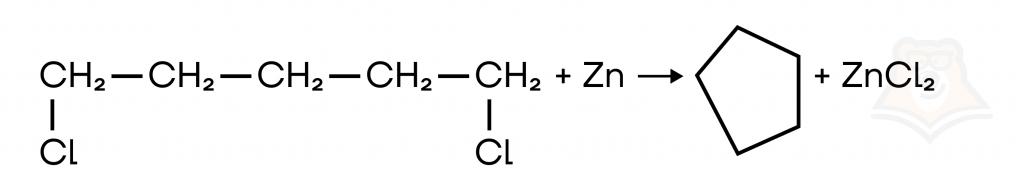
| Для чего могут применяться галогенпроизводные углеводородов? Галогенпроизводные имеют широкий спектр применения.Они не только выступают в качестве сырья для синтеза множества органических соединений, но и находят применение в различных сферах промышленности. Галогенпроизводные используются в строительстве в качестве растворителей, масел и смазочных материалов, а также могут применяться при производстве тканей и красителей, резины и каучуков. В сельском хозяйстве галогенпроизводные применяются в качестве пестицидов и инсектицидов. В медицине галогеналканы используются как средства для наркоза. |
Сегодняшняя статья заканчивается, пора выбрать главным героем новый класс органических веществ и погрузиться в новую тему. Для продолжения приключения по органической химии рекомендуем познакомиться со спиртами, а сделать это можно, прочитав статью «Предельные одноатомные и многоатомные спирты, фенол».

Термины
Ароматические углеводороды — вещества, в молекулах которых содержится одно или несколько бензольных колец.
Непредельные углеводороды — это углеводороды, в молекулах которых имеются атомы углерода, связанные между собой двойными или тройными связями.
Предельные углеводороды — это углеводороды, в молекулах которых имеются только одинарные связи.
Фактчек
- Галогенпроизводные — класс органических веществ, в которых атом водорода замещен на галоген.
- Галогенпроизводные классифицируются по количеству атомов галогенов, по тому, какой галоген в составе, а также по типу углеводорода.
- Названия галогенпроизводных составляется по принципу «номера позиций радикалов через запятую арабскими цифрами — приставка, отражающая количество атомов галогенов + название галогена + имя углеродной цепочки».
- К способам получения галогенпроизводных относятся галогенирование предельных и непредельных углеводородов, гидрогалогенирование непредельных углеводородов и замещение спиртовой группы на галоген.
- Галогенпроизводные вступают в реакции замещения, дегидрогалогенирования, реакции Вюрца и Фриделя-Крафтса и дегалогенирования.
Проверь себя
Задание 1.
К каким группам относится хлорметан?
- Хлорпроизводное, дигалогенпроизводное, предельное соединение
- Бромпроизводное, моногалогенпроизводное, предельное соединение
- Хлорпроизводное, моногалогенпроизводное, непредельное соединение
- Хлорпроизводное, моногалогенпроизводное, предельное соединение
Задание 2.
Каким образом может быть получен бромэтан?
- Бромирование этана в темноте
- Бромирование этилена
- Добавление бромоводорода к этену
- Бромирование метанола
Задание 3.
Какое соединение не вступает с 1,2-дихлорпропаном в реакцию замещения?
- Водный раствор щелочи
- Спиртовой раствор щелочи
- Аммиак
- Нитрит серебра
Задание 4.
Какой продукт образуется при дегидрогалогенировании 1,2-дихлорбутана?
- Бутен-1
- Бутен-2
- Бутин-1
- Бутин-2.
Задание 5.
Какой металл используется при дегалогенировании дигалогенпроизводных?
- Кальций
- Магний
- Калий
- Марганец
Ответы: 1. — 4; 2. — 3; 3. —2; 4. — 3; 5. — 2.

 к списку статей
к списку статей




