
На этой странице вы узнаете
- Из чего делают гидрокостюмы?
- Полимеры повсюду — где и как мы сталкиваемся с продуктами полимеризации алкадиенов?
Оказывается, органика настолько логична, что уже по названию темы можно сделать выводы о строении веществ и их химических свойствах. Сегодня мы с вами научимся это делать, а заодно поговорим об алкадиенах.
Общая характеристика алкадиенов
Алкадиены — непредельные (то есть имеющие кратные связи) углеводородные соединения, которые содержат две двойные связи между атомами углерода.
Подробнее про кратные связи можно прочитать в статье: «Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа».
Общая формула алкадиенов выглядит так: СnH2n-2.
Как вы можете заметить, общая формула алкадиенов совпадает с общей формулой алкинов, а значит, они будут друг для друга межклассовыми изомерами.
Давайте рассмотрим строение алкадиенов на примере молекулы дивинила, то есть бутадиена-1,3.
Атомы углерода, участвующие в образовании двойных связей, находятся в состоянии sp²-гибридизации. Остальные атомы углерода (если они есть) находятся в состоянии sp³-гибридизации.
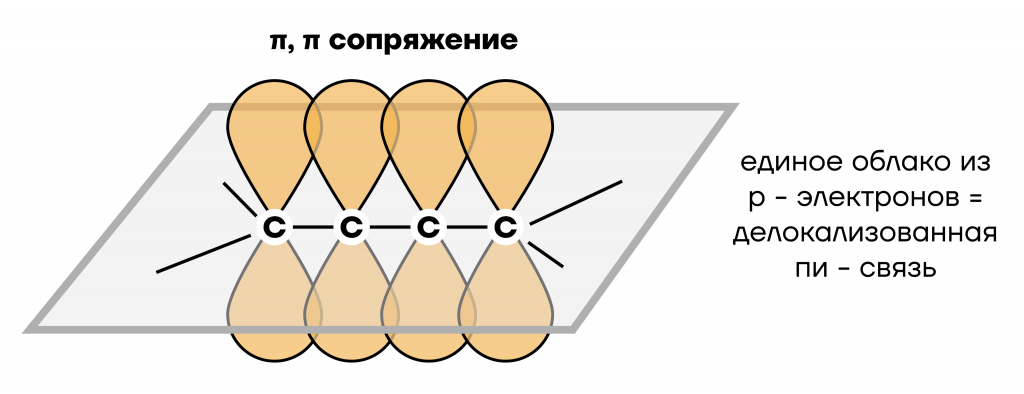
Молекула бутадиена-1,3 содержит четыре атома углерода в sp2—гибридизованном состоянии.
π-электроны двойных связей образуют единое электронное облако (сопряженную систему) и делокализованы (равномерно распределены) между всеми атомами углерода.
На изображении видно, что форма молекулы плоская, то есть все атомные орбитали «лежат» на одной поверхности.
А чему равен валентный угол и длина связи алкадиенов? 120° и 0,137 нм соответственно.
Выделяют три типа алкадиенов: сопряженные, кумулированные и изолированные. Все эти виды отличаются друг от друга лишь положением двойных связей.
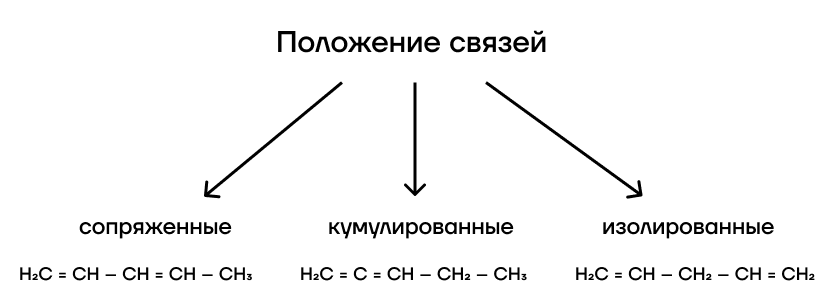
- Сопряженные связи разделены между собой одной одинарной связью.
- Кумулированные расположены у одного атома углерода.
- Изолированные связи разделены двумя и более одинарными связями.
Положение связей играет важную роль для алкадиенов и определяет их химические свойства.
Гомологами алкадиенов будут алкадиены, которые имеют такое же расположение двойных связей, но отличаются на одну или несколько CH2-групп. Например, на иллюстрации ниже изображен бутадиен-1,3, под которым находится пентадиен-1,3.
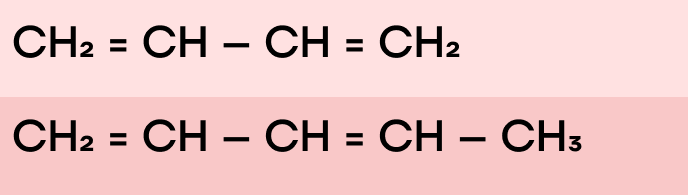
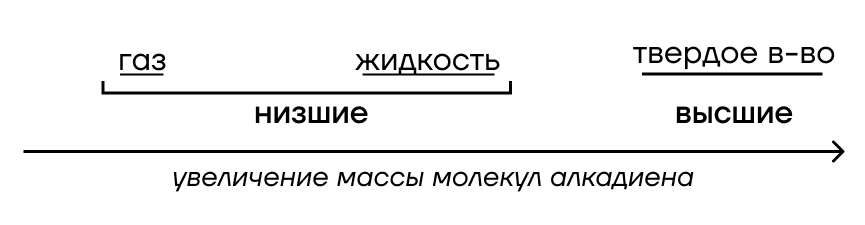
Физические свойства схожи с алкенами: с увеличением числа атомов углерода происходит переход сначала из газов в жидкость, а потом из жидкости в твердое агрегатное состояние.
Теперь рассмотрим, какие виды изомерии характерны для алкадиенов. В принципе, для алкадиенов характерны все уже привычные нам виды изомерии. Но есть один, который встречается не у всех органических веществ — это цис- и транс-изомерия. Алкадиены, в которых одинаковые заместители располагаются по одну сторону от плоскости двойной связи — цис-изомеры. Алкадиены, в которых одинаковые заместители располагаются по разные стороны от плоскости двойной связи — транс-изомеры.
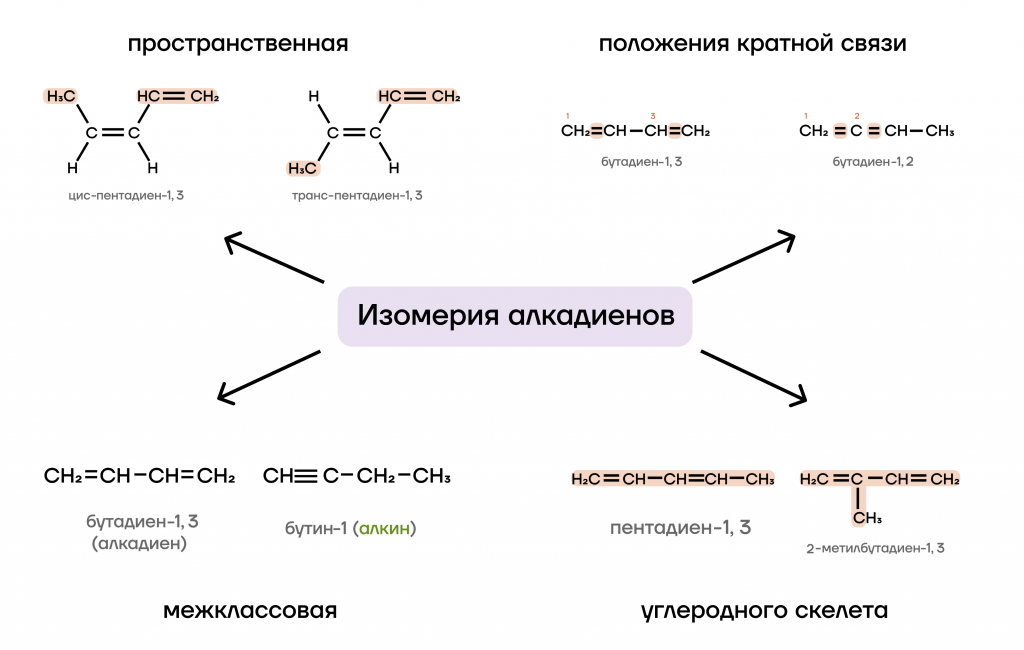
Номенклатура у алкадиенов простая, к названию углеводорода прибавляется суффикс «-диен». Стоит запомнить пару тривиальных названий, которые часто встречаются:

Химические свойства алкадиенов
Химические свойства диенов очень схожи со свойствами алкенов, для них также характерны реакции присоединения за счет разрыва пи-связей. Но делокализация электронной плотности у сопряженных алкадиенов добавляет им некоторые особые свойства.
- Галогенирование.
Галогенирование у алкадиенов благодаря системе сопряженных связей может иметь несколько вариантов развития событий.
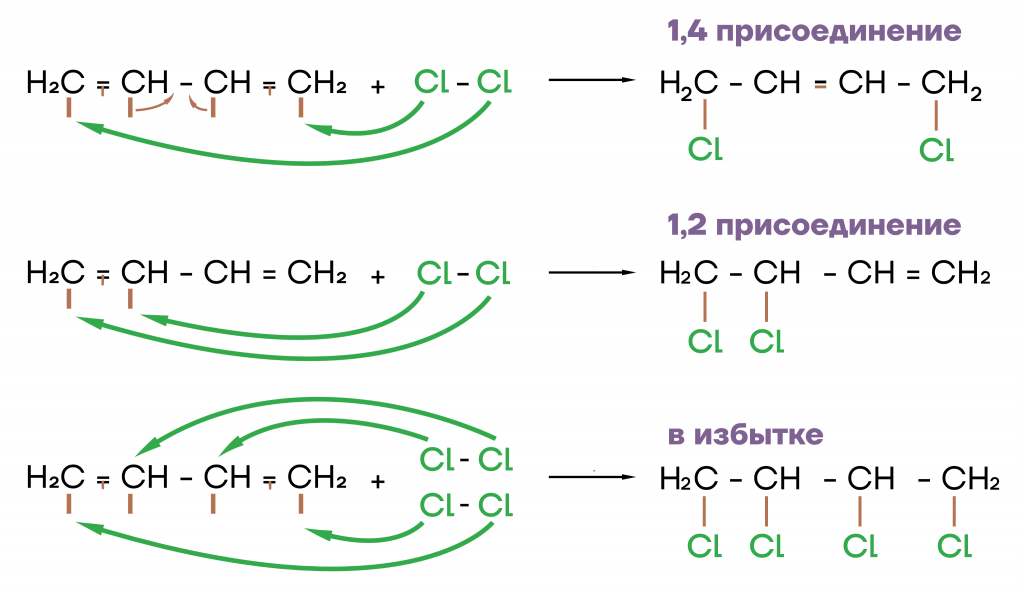
Например, в случае с дивинилом, может произойти как 1,4-присоединение (преимущественно), так и 1,2-присоединение и даже тетрахлорпроизводное в избытке хлора.
Для удобства молекулу галогена лучше расписывать на атомы, так будет намного проще понять, как именно будет протекать данная реакция.
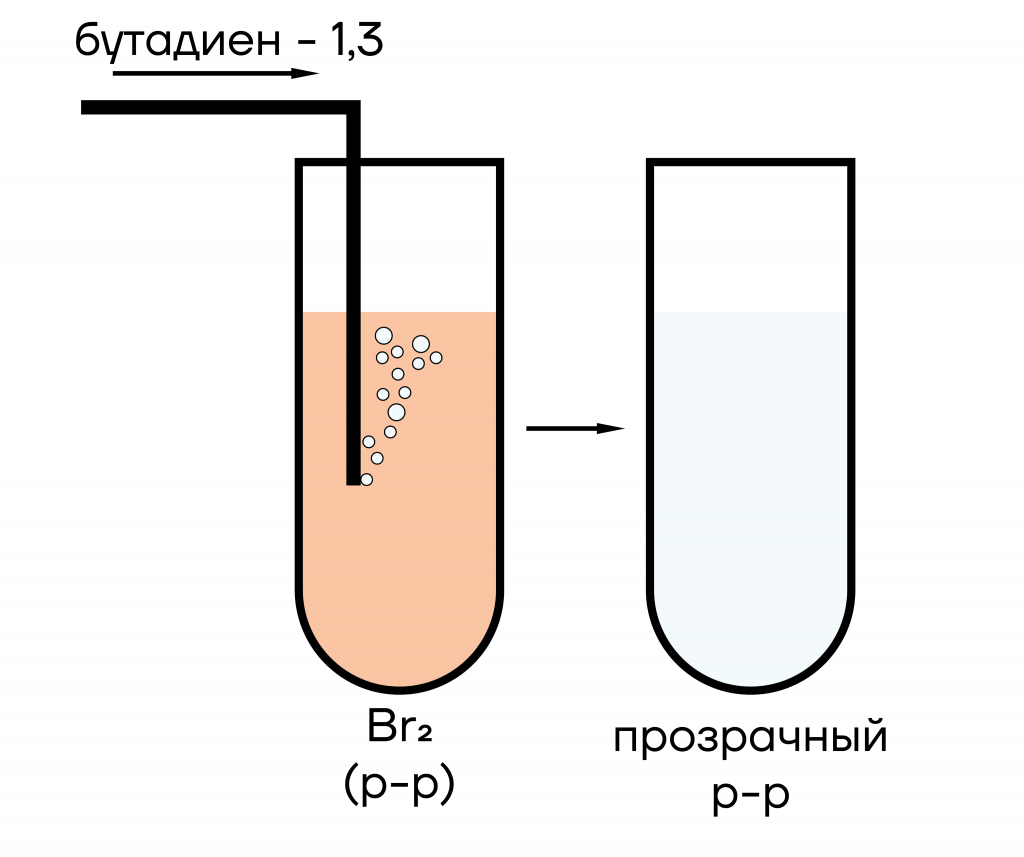
Важно: реакция с бромной водой считается качественной, так как происходит обесцвечивание раствора.
| Из чего делают гидрокостюмы? Из бутадиена галогенированием получают хлоропрен, а из него уже неопрен. Этот мягкий пористый материал используется для изготовления гидрокостюмов для подводного плавания и дайвинга. А первый такой костюм был создан в 1953 году французским изобретателем Жоржем Бюша. |

- Гидрирование.
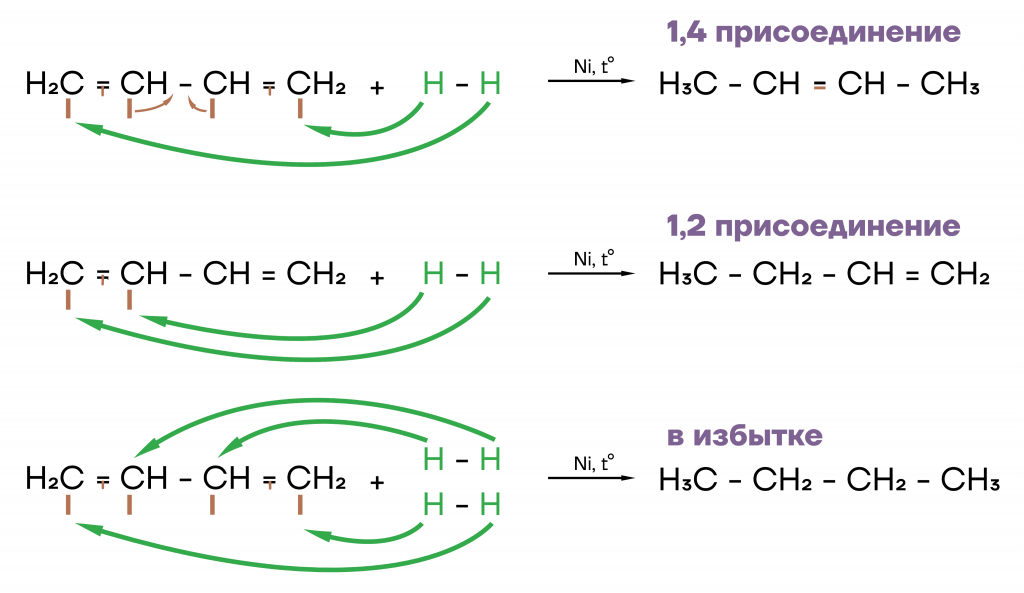
Водород присоединяется к углеродам, которые находятся по бокам от кратных связей. Аналогично галогенированию, возможны разные варианты присоединения.
- Гидрогалогенирование.
Гидрогалогенирование происходит по правилу Марковникова: водород присоединяется к более гидрированному атому углерода, а галоген к менее гидрированному.
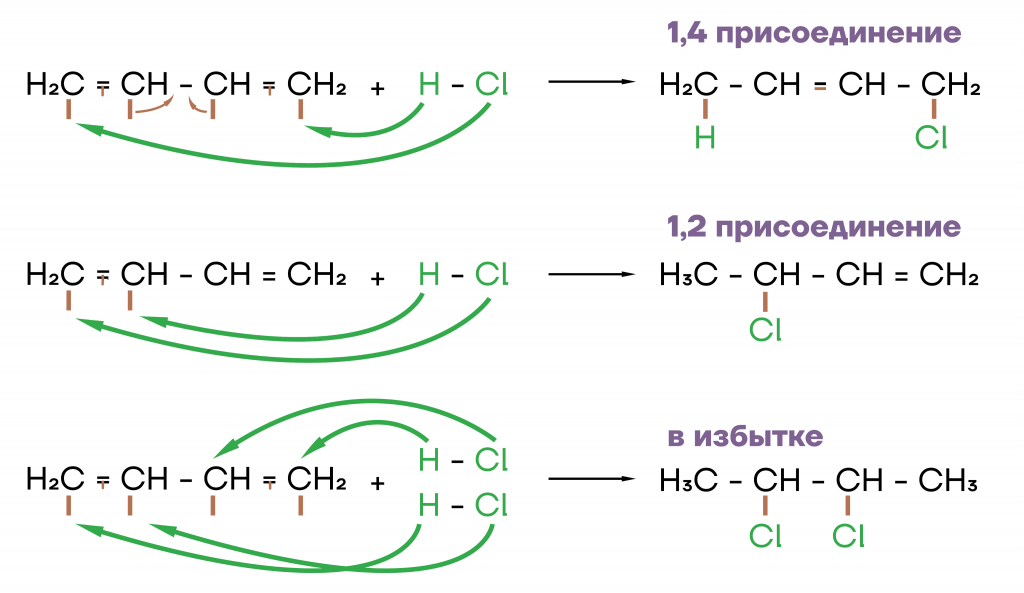
Опять же возможны разные исходы, но преимущественно идет 1,4-присоединение.
- Полимеризация.
Из мономера путем полимеризации мы можем получить полимер — вещество, которое состоит из повторяющихся звеньев — мономеров, как бусы из одинаковых бусинок.
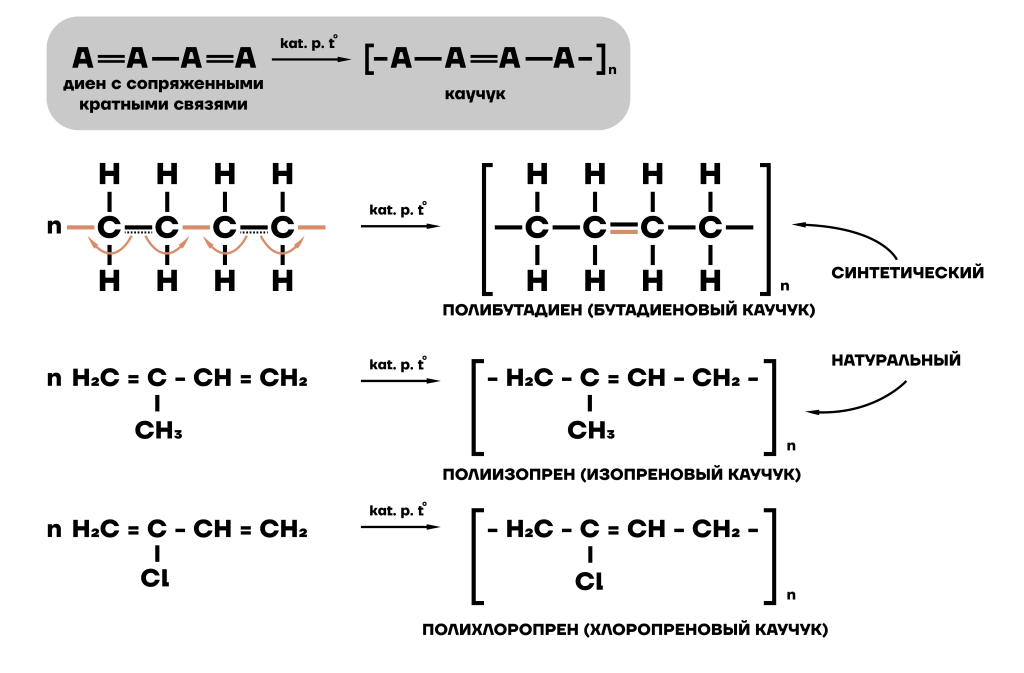
Продукт полимеризации бутадиена — синтетический каучук, а изопрена — натуральный.
Из каучука в дальнейшем получают более прочную резину путем вулканизации. Цепочки полимеров как бы сшиваются между собой атомами серы.
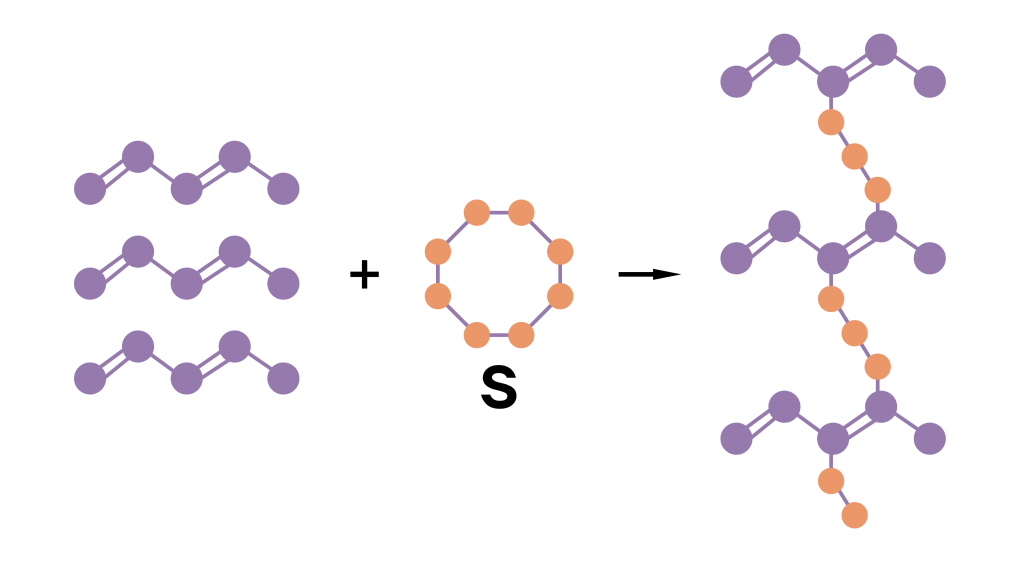
| Полимеры повсюду — где и как мы сталкиваемся с продуктами полимеризации алкадиенов? Вы когда-нибудь задумывались, где и как применяется каучуки? Каучук является очень популярным сырьем для изготовления всевозможных изделий из резины. Спрос на каучук в несколько раз превышает объемы его производства. Из него делают автомобильные шины, конвейерные ленты, резиновую обувь, подошву для обуви, клей, детские игрушки. В природе натуральный каучук содержится в дереве Гевея. Одно такое дерево производит около 8 кг каучука в год. Индейцы из Южной Америки обмакивали ноги в горячий сок дерева и ждали, когда он застынет — в результате получалась прочная и непромокаемая обувь. |
- Окисление.
а) мягкое — рвутся только пи-связи и образуются четырехатомные спирты. Раствор перманганата калия при этом обесцвечивается.
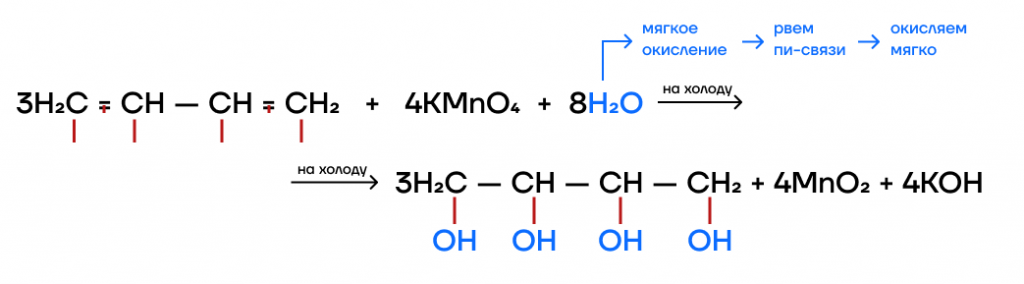
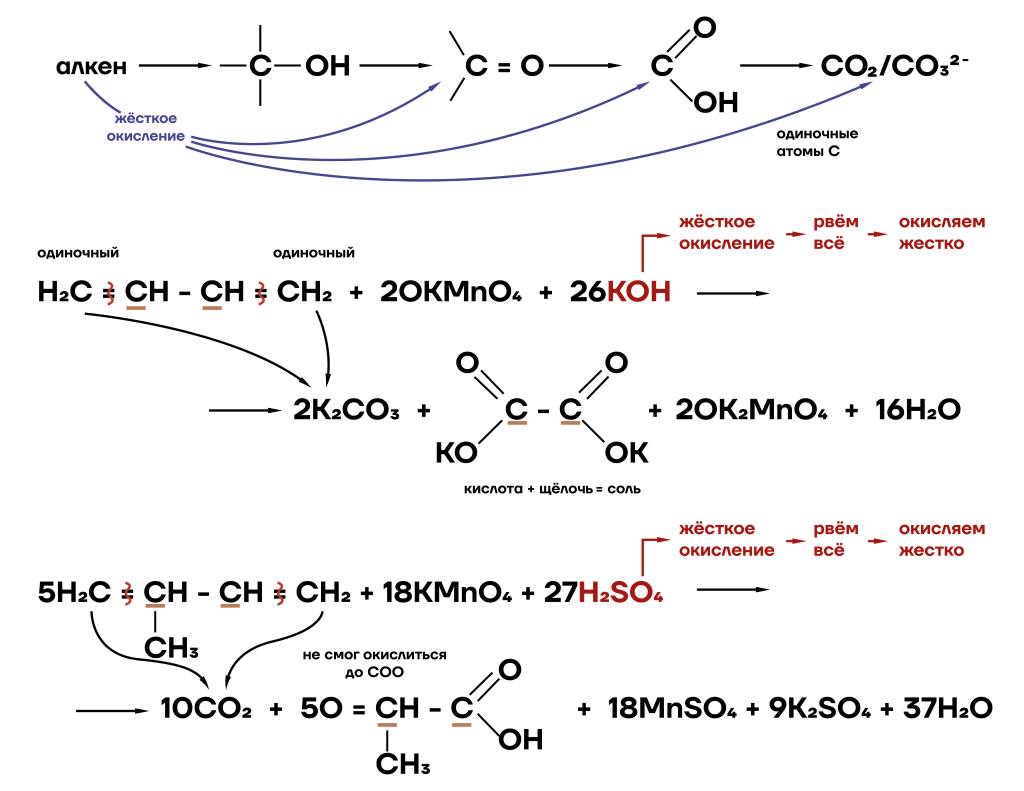
б) жесткое — рвутся и пи-, и сигма-связи.
В щелочной среде образуются соли карбоновых кислот, в кислой — карбоновые кислоты и их производные.
- Горение.
Здесь все просто, все углеводороды горят до углекислого газа и воды.
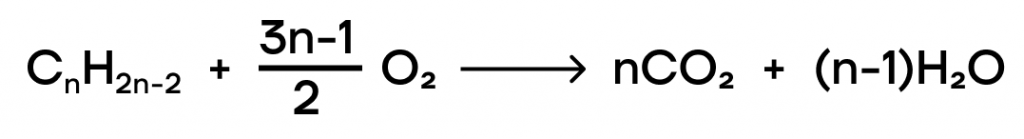
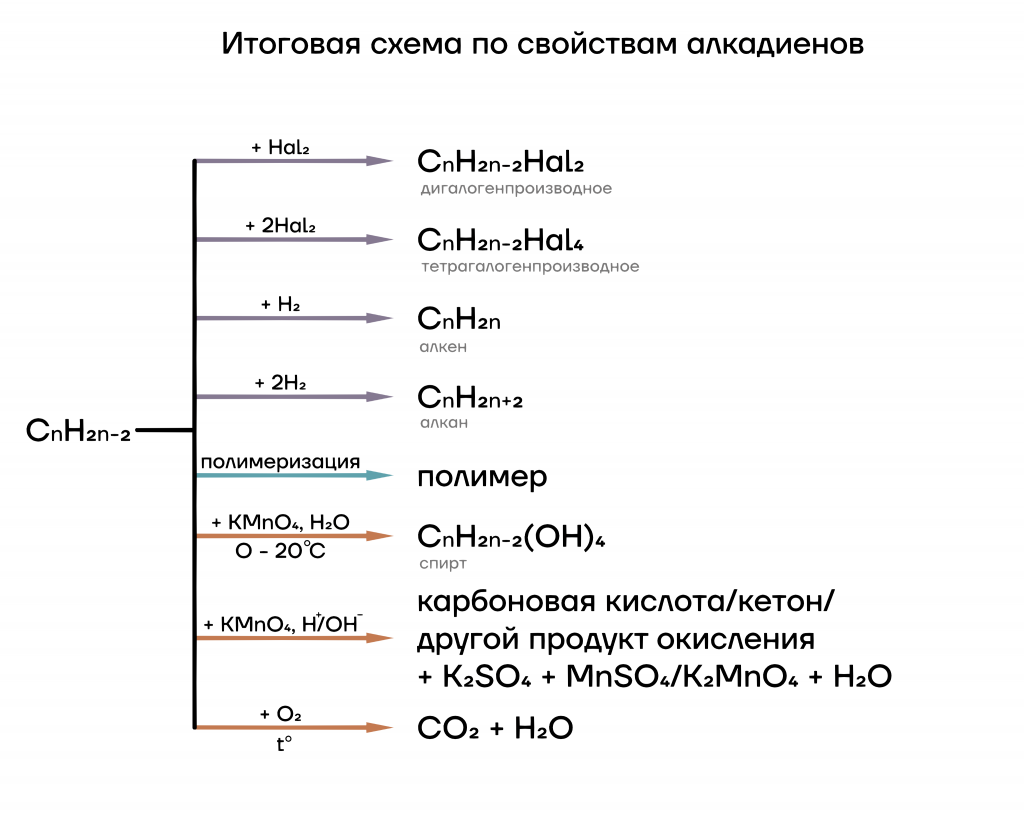
Давайте подведем итог, с чем же реагируют алкадиены. В этом нам поможет вот такая схема:
Получение алкадиенов
Алкадиены получают для того, чтобы из них синтезировать каучуки: покрышки, ластики, резиновые сапоги и перчатки, канцелярские резинки и так далее.
- В лаборатории.
Есть несколько способов, но все они требуют достаточно жестких условий, так как для протекания реакции обязательно должны быть катализаторы и температура. Давайте рассмотрим некоторые способы получения алкадиенов в лаборатории.
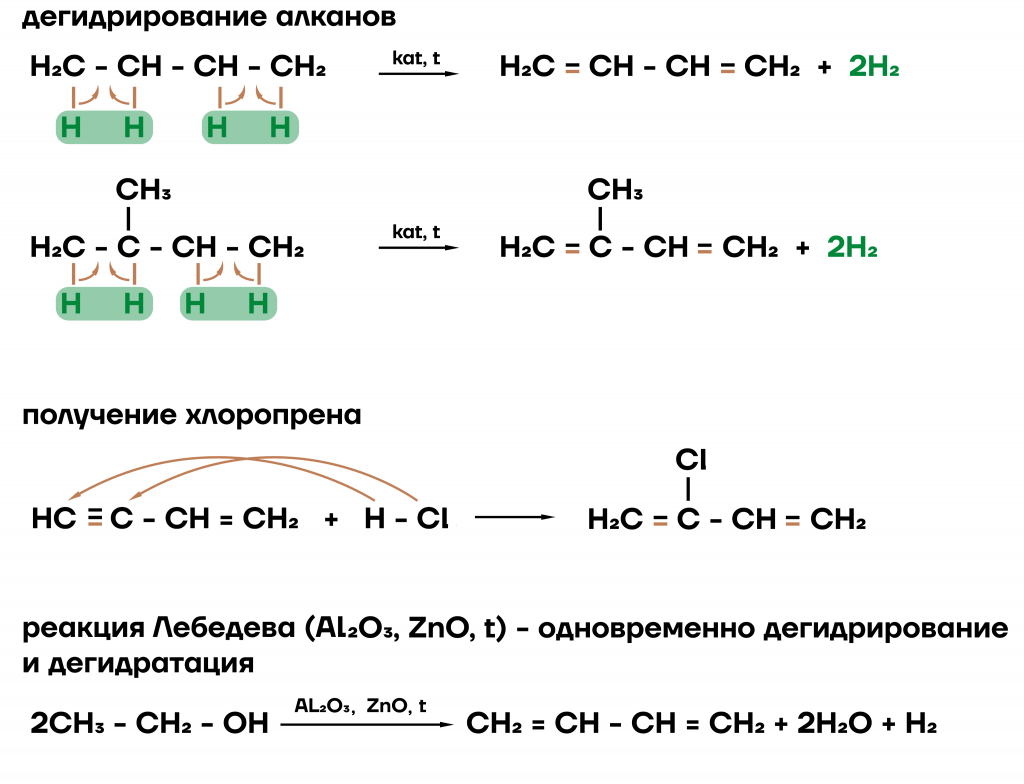
- В промышленности.
В промышленности алкадиены получают либо из спиртов под действием серной кислоты, которая не расходуется в течение реакции, либо из дигалогеналканов.
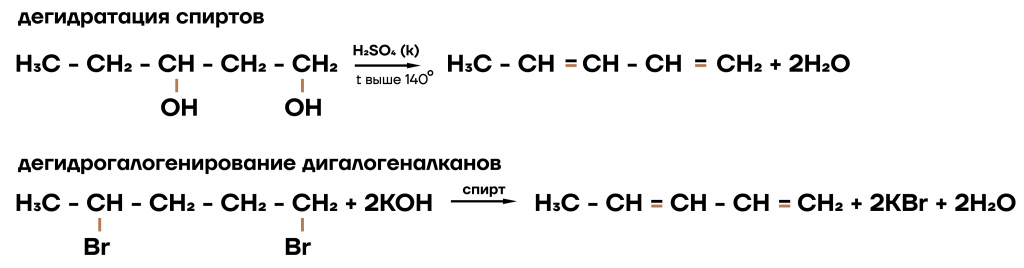
Вот мы и изучили все свойства алкадиенов. Как вы уже могли заметить, они довольно схожи с алкенами, но при этом имеют свои очень интересные особенности.
Фактчек
- Алкадиены — непредельные углеводородные соединения, которые содержат две двойные связи.
- Общая формула алкенов выглядит так: СnH2n−2.
- Валентный угол и длина связи равны 120° и 0,137 нм соответственно.
- Гомологами алкадиенов будут алкадиены, которые имеют такое же расположение двойных связей, но отличаются на одну или несколько CH2-групп.
- Для алкадиенов характерны реакции с галогенами, водородом, галогеноводородами, с кислородом, а также полимеризация, мягкое и жесткое окисление.
- Получают диены двумя способами: лабораторным и промышленным.
Проверь себя
Задание 1.
Что является алкадиеном?
- дивинил
- ацетилен
- пропан
Задание 2.
С чем не реагируют алкадиены?
- с бромом
- с кислородом
- с алканами
Задание 3.
С чем реагирует дивинил?
- с хлороводородом
- с метаном
- с бензолом
Задание 4.
Бутадиен-1,3 является изомером…
- пентадиена-1,3
- пентадиена-1,2
- пентена-3
Задание 5.
Алкадиены применяют для изготовления…
- красителей
- мебели
- резины
Ответы: 1. — 1; 2. — 3; 3. — 1; 4. — 1; 5. — 3.

 к списку статей
к списку статей




