
На этой странице вы узнаете
- Красота в молекулах: какой из широко известных пигментов содержит карбонильные группы?
- Одна известная тайна: что сделало Шанель №5 особенным ароматом?
- Что хранят в формалине?
В этой статье мы с вами найдем новых приятелей, с которыми обязательно нужно подружиться, чтобы хорошо понимать и знать химию. Их зовут карбонильными соединениями — альдегидами и кетонами.
Строение альдегидов и кетонов
Альдегиды и кетоны — органические соединения, которые содержат одну и ту же функциональную группу — карбонильную группу.
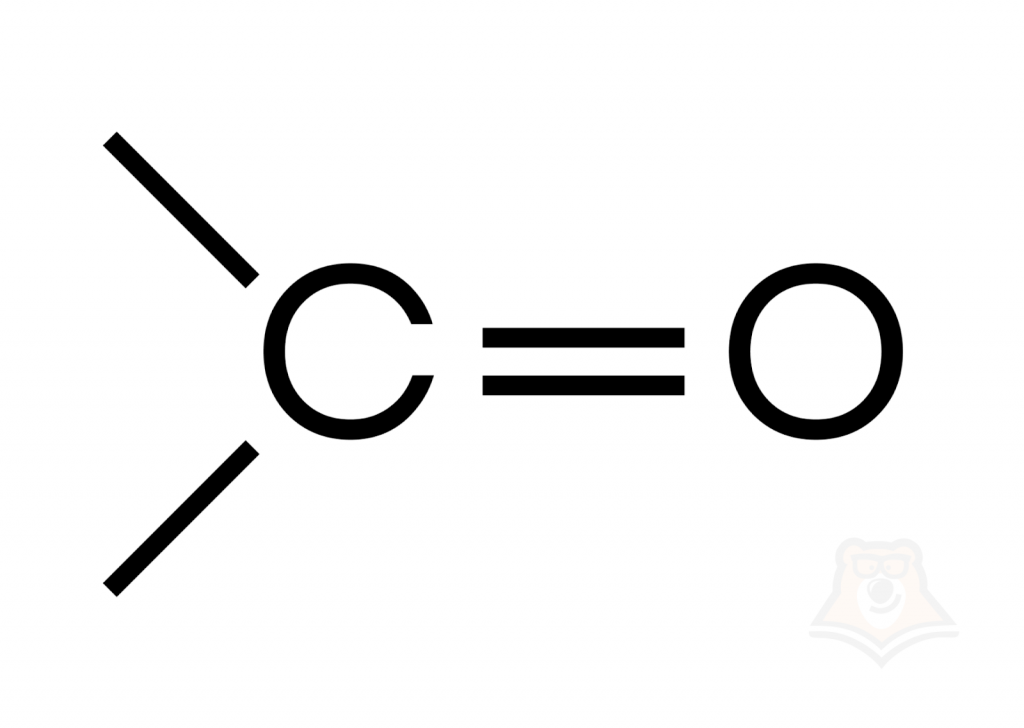
Общая формула альдегидов и кетонов одинаковая: СnH2nО.
Чем же отличаются альдегиды и кетоны?
Альдегиды — органические соединения, в которых карбонильная группа связана с одним углеводородным радикалом и с одним атомом водорода.
Кетоны — органические соединения, в которых карбонильная группа связана с двумя углеводородными радикалами.

| Красота в молекулах: какой из широко известных пигментов содержит карбонильные группы? Индиго — это природный краситель, получаемый из растений, в своей структуре содержит две карбонильные группы С=O. Индиго был одним из самых дорогих красителей в истории. В древности он был ценен, так как для его получения требовалось большое количество растений. Индиго использовался древними цивилизациями, такими как Древний Египет и Индия, для окрашивания тканей в глубокий синий цвет. Известно, что в Древнем Египте индиго использовалось для окрашивания погребальных пеленок и одежды фараонов. Индиго считается одним из самых стойких красителей, которые не выцветают со временем. Это объясняет его популярность в текстильной промышленности. Синий цвет, получаемый из индиго, имеет символическое значение во многих культурах. Он ассоциируется с мудростью, духовностью и гармонией. |
Теперь давайте рассмотрим строение альдегидов и кетонов.
Кислород оттягивает на себя электронную плотность за счет того, что он более электроотрицательный элемент, поэтому приобретает частично отрицательный заряд (𝛿-), а углерод частично положительный (𝛿+), связь становится полярной. Радикалы с +I эффектом делают связь менее полярной, таким образом происходит снижение химической активности.

Подробнее про электронные эффекты заместителей мы рассказывали в статье «Теория строения органических соединений».
Гомологи альдегидов и кетонов
Гомологи (гомо- «одинаковый, схожий») — соединения, относящиеся к одному классу веществ, отличающиеся длиной углеводородного скелета на одну или несколько групп -СH2— (гомологическую разность).
Соответственно, гомологи альдегидов и кетонов — альдегиды и кетоны с одинаковым расположением карбонильной группы, но отличаются на одну или несколько -CH2-групп. Часть гомологического ряда альдегидов, начиная с первого представителя, представлена на изображении ниже.

Теперь рассмотрим несколько первых представителей гомологического ряда кетонов.

Мы узнали, как выглядят гомологи альдегидов и кетонов. Далее нам необходимо научиться правильно их называть, используя номенклатуру.
Номенклатура альдегидов
По систематической номенклатуре цепь нумеруется, начиная с углеродного атома, который является частью альдегидной группы, и добавляется окончание «-аль» к названию алифатического углеводорода. Обычно номер не указывается в названии рядом с альдегидной группой.

Чтобы составить название разветвленного альдегида, необходимо пронумеровать главную цепь (она обязательно должна включать в себя карбонильную группу), определить название алкана, который соответствует длине цепи (количеству атомов углерода). Затем, формируя название соединения, перечислить в алфавитном порядке радикалы, которые не относятся к главной цепи с цифрами, обозначающими их расположение, назвать главную цепь и добавить к ней суффикс «-аль».
Давайте рассмотрим пример:

Главная цепь состоит из шести атомов углерода. Соответствующий алкан — гексан. Третий, четвертый и пятый атомы углерода главной цепи связаны с этильным и двумя метильными радикалами.
Составим название альдегида — 4,5-диметил-3-этилгексаналь.
Для альдегидов существуют тривиальные названия, которые формируются исходя из соответствующей карбоновой кислоты, до которой может окислиться альдегид.
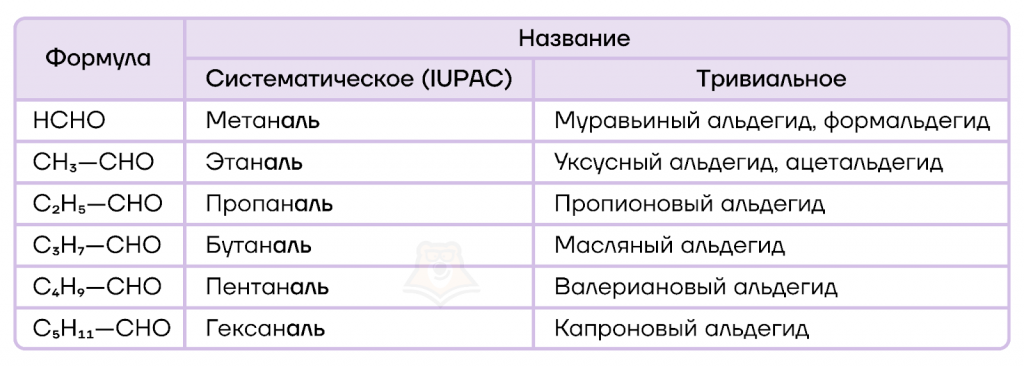
Номенклатура кетонов
По систематической номенклатуре названия кетонов формируются аналогичным образом, что и у альдегидов, только здесь мы добавляем суффикс «-он» к названию главной цепи и указываем цифрой местоположение кислорода из карбонильной группы.
Рассмотрим пример. Соединение на рисунке ниже в главной цепи содержит 4 атома углерода, соответствующий алкан — бутан. В третьем положении также содержится заместитель метил. Формируя название, сначала указываем цифрой местоположение радикала и его название — «3-метил», затем указываем название основной цепи, прибавляя к названию соответствующего алкана суффикс «-он», и указываем цифрой местоположение кислорода — 2. Таким образом, получаем название соединения 3-метилбутанон-2.

Еще пара примеров формирования названий по систематической номенклатуре.

Также возможно формирование названий кетонов по радикально-функциональной номенклатуре. Кетоны называют, перечисляя заместители при кетогруппе в алфавитном порядке, добавляя слово «кетон». Названия заместителей необходимо знать наизусть. Наиболее распространенные радикалы и их названия мы описываем в статье «Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа».
Например, кетон, который содержит в качестве заместителей два метила у кетогруппы, по радикально-функциональной номенклатуре будет называться диметилкетон. На втором примере мы видим, что у кетогруппы содержится два заместителя — метил и этил. Перечисляем их в алфавитном порядке, добавляем в конце слово «кетон» и получаем название метилэтилкетон.
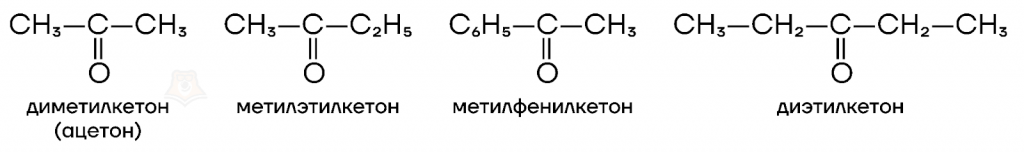
Для некоторых кетонов используют тривиальные названия.
Например, ацетон. Он же пропанон-2 по систематической номенклатуре, диметилкетон — по радикально-функциональной номенклатуре.

Давайте узнаем, какими физическими свойствами обладают альдегиды и кетоны.
Физические свойства альдегидов и кетонов
Нужно знать, что с увеличением числа атомов углерода происходит переход из газообразного состояния в жидкое, а затем в твердое.
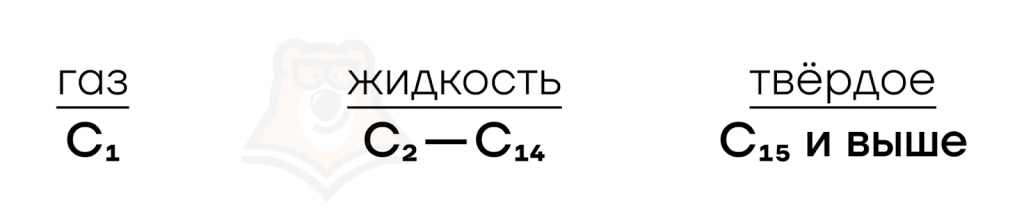
Низшие альдегиды (углеводородная цепь состоит из 1-7 атомов углерода) имеют неприятный резкий запах. Высшие альдегиды — альдегиды, содержащие 8-12 атомов С в углеводородной цепи — душистые вещества.
Альдегиды с 1-3 атомами С хорошо растворяются в воде, с увеличением числа атомов С растворимость уменьшается. Все альдегиды растворяются в органических растворителях.
Альдегиды раздражают слизистые оболочки глаз и верхних дыхательных путей, могут негативно влиять на нервную систему.
| Одна известная тайна: что сделало Шанель №5 особенным ароматом? Первые духи, в составе которых были использованы альдегиды — это именно Шанель №5. Аромат был представлен в 1921 году. Коко Шанель, создательница аромата, смело включила альдегиды в формулу, чтобы достичь новаторского эффекта и создать уникальный запах, отличающийся от привычных на тот момент парфюмов. Точный состав духов является коммерческой тайной. С тех пор альдегидные ноты стали важной и отличительной чертой Шанель №5, а также вдохновением для многих ароматов. Выше, в физических свойствах мы уже упоминали, что альдегиды, в составе которых от 8 атомов углерода — душистые вещества, то есть обладают приятным запахом. Диапазон ароматов у альдегидов широк, например, деканаль (C10H20O) — запах апельсиновой корки, мирценаль (C14H28O) — цветочный аромат. Альдегиды играют важную роль в мире парфюмерии, внося свою характерность и свежесть в ароматы. Их использование требует владения балансом в аромате и мастерства, чтобы создавать гармоничные и запоминающиеся композиции. |
Далее рассмотрим изомеры и виды изомерии альдегидов и кетонов.
Изомерия альдегидов и кетонов
Изомеры — вещества, имеющие одинаковый качественный и количественный состав, но разное строение и свойства.
Для альдегидов и кетонов характерны следующие виды изомерии.
- Углеродного скелета
Бутаналь имеет линейную структуру, а изобутаналь — разветвленную. У веществ одинаковое расположение карбонильной группы, отличается углеводородный скелет.
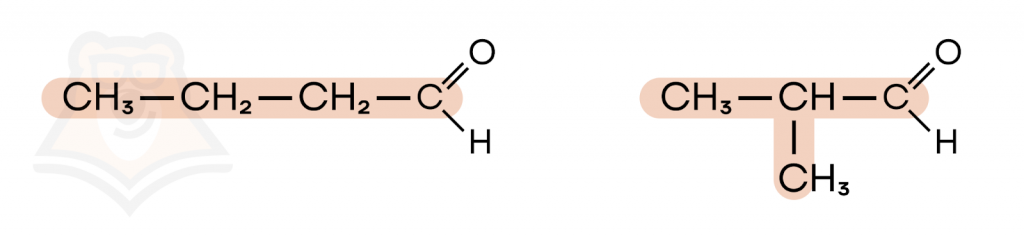
- Положения карбонильной группы
Данный вид изомерии характерен только для кетонов. Вещества с одинаковой химической формулой различаются в строении в зависимости от положения карбонильной группы.
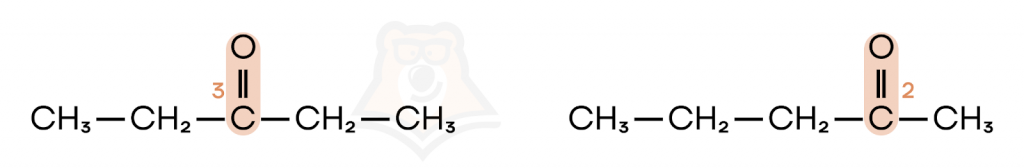
- Межклассовая изомерия
Альдегиды и кетоны изомерны друг другу.

Мы рассмотрели все виды изомерии, характерные для альдегидов и кетонов. Теперь изучим их химические свойства.
Химические свойства карбонильных соединений
Благодаря наличию у карбонильных соединений двойной связи между углеродом и кислородом, для них характерны реакции присоединения по двойной связи. На углероде в карбонильной группе сосредоточен частично положительный заряд δ+, а на кислороде — частично отрицательный δ-, поэтому к углероду присоединяется отрицательно заряженная часть молекулы — анион, а к кислороду — положительно заряженная часть молекулы — катион. При этом альдегиды вступают в реакции присоединения легче, чем кетоны.
а) Реакции присоединения.
- Гидрирование.
В присутствии никеля альдегиды при взаимодействии с водородом образуют первичные спирты, кетоны — вторичные, а соединения, содержащие несколько карбонильных групп — многоатомные спирты.

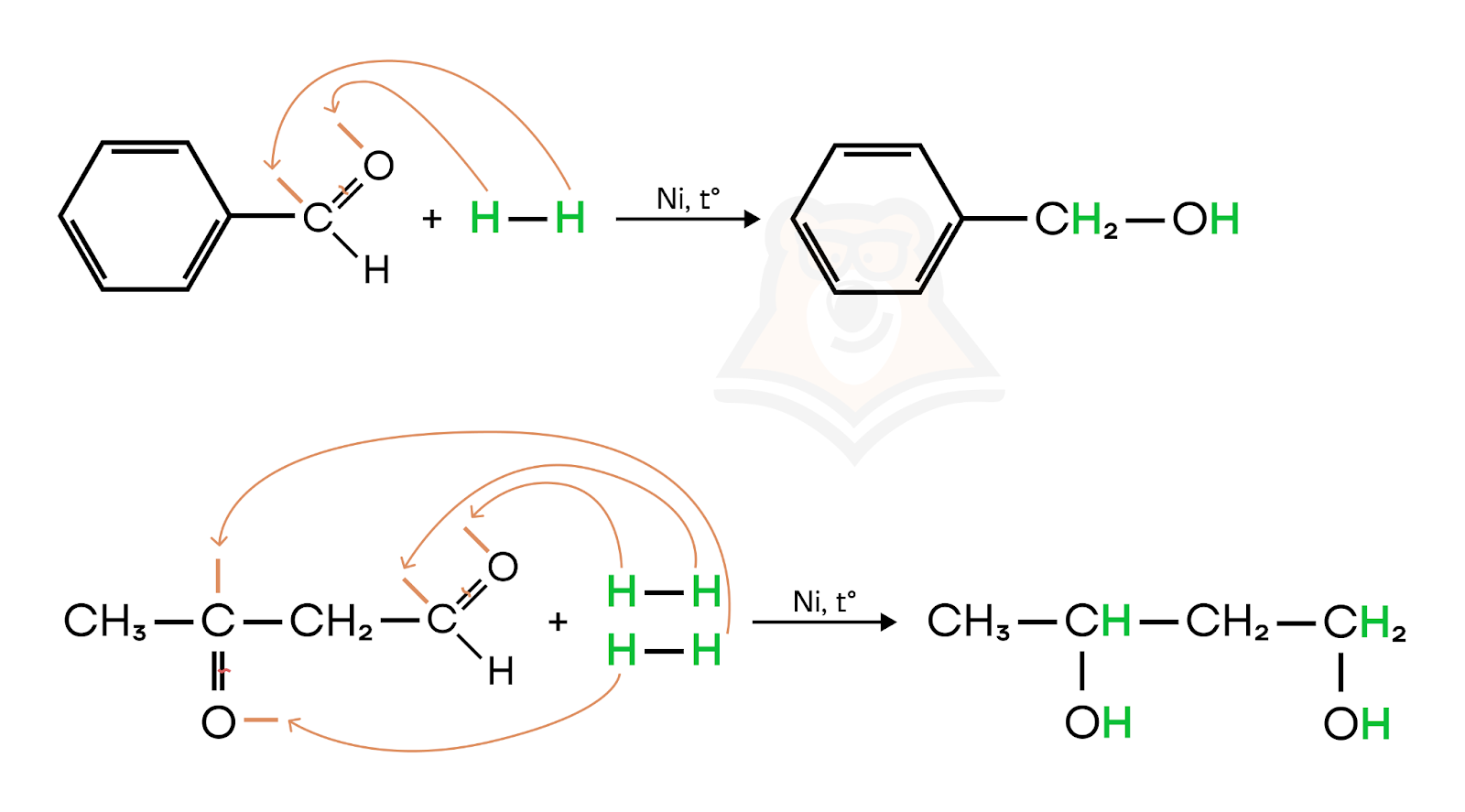
- Гидратация.
При присоединении воды к альдегидам образуются геминальные диолы — двухатомные спирты, в которых обе OH-группы находятся у одного атома углерода. Геминальные диолы очень неустойчивы и существуют только при низких температурах.


- Реакция со спиртами.
Присоединение спиртов к альдегидам приводит к образованию полуацеталей — соединений, в которых атом углерода связан с гидроксильной (-OH) и алкоксильной (-OR) группами. Такие полуацетали могут прореагировать со спиртами еще раз, и тогда мы уже получим ацетали — соединения, в которых атом углерода связан с двумя алкоксильными группами.
Алкоксильные группы представляют собой функциональные группы состава -OR, где О — кислород, а R — алкильный радикал.

- Присоединение синильной кислоты.
При присоединении к карбонильным соединениям синильной кислоты HCN в структуре полученных соединений появляются две функциональные группы: -ОН и -CN, образуются циангидрины (гидроксинитрилы).
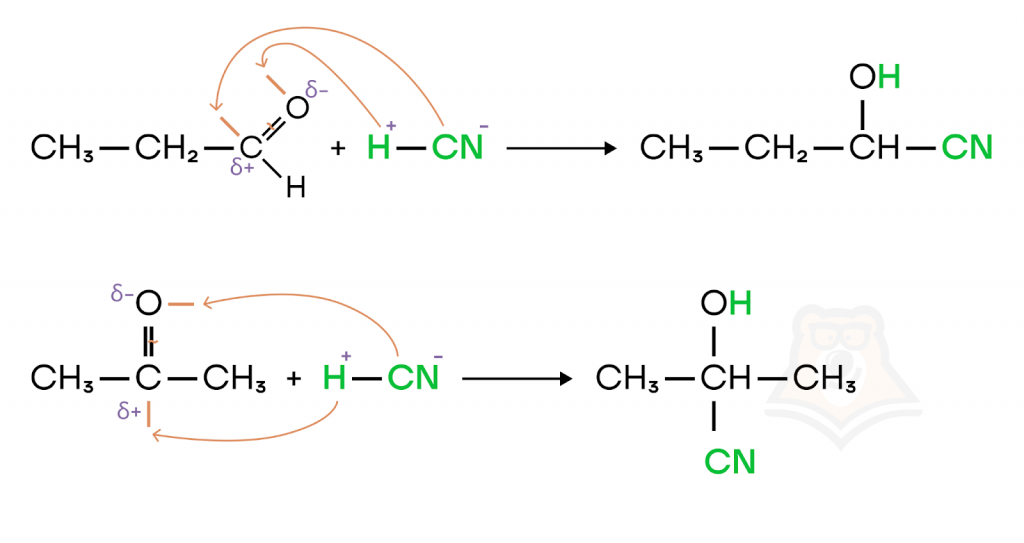

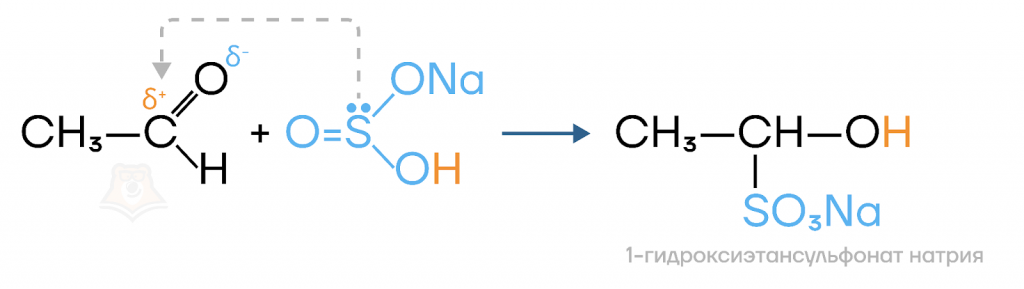
- Присоединение гидросульфита натрия.
Качественная реакция на альдегиды и кетоны. Реакцию проводят с насыщенным раствором гидросульфита натрия и наблюдают выпадение белого кристаллического осадка.
б) Полимеризация.
Полимеризация характерна для низших альдегидов.

Кетоны не полимеризуются.
- Полимеризация низших альдегидов.
Полимеризация формальдегида имеет промышленное значение. Реакция протекает в присутствии катализатора — минеральной кислоты. Получается полиформальдегид, называемый также параформ.

- Поликонденсация фенола с метаналем.
Поликонденсация — процесс, при котором молекулы двух веществ соединяются в длинные цепи с образованием побочных низкомолекулярных продуктов, например, воды.
Поликонденсация похожа на реакцию полимеризации, образуются полимеры. Отличие заключается в том, что в результате реакции поликонденсации помимо полимера получаются еще низкомолекулярные продукты, например вода, то есть в результате реакции поликонденсации образуется два продукта.
Например, формальдегид вступает в такую реакцию с фенолом. В результате реакции образуются фенолформальдегидная смола и вода.
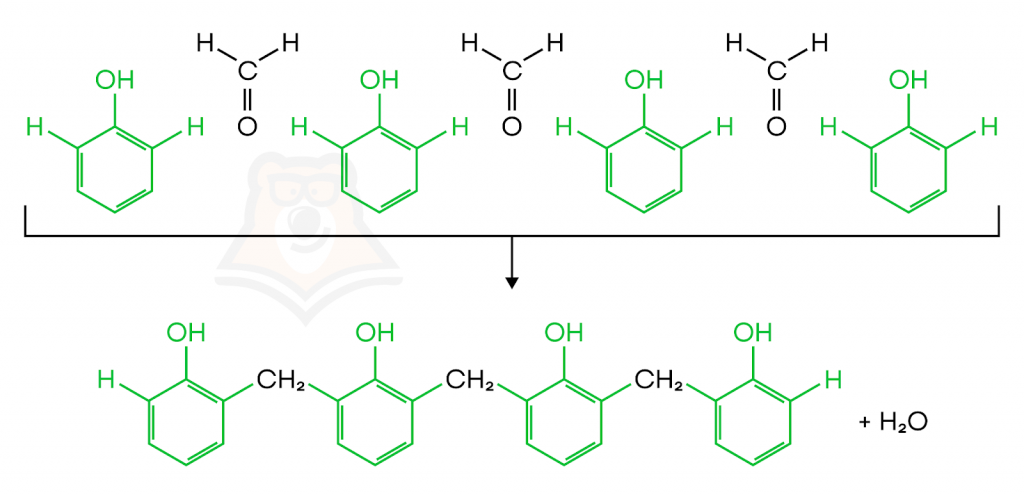
Общий вид уравнения реакции:
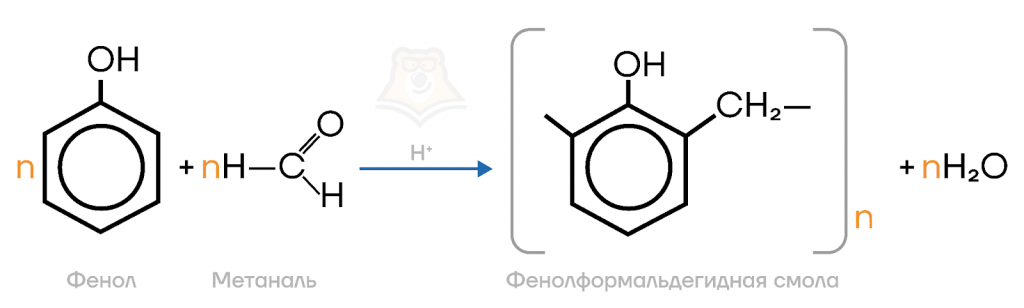
в) Реакции замещения.
- Галогенирование.
Карбонильные соединения вступают в реакции замещения с галогенами с образованием галогенпроизводных.

Важно: галоген замещается в альфа-положение (ближайший к карбонильной группе атом углерода).
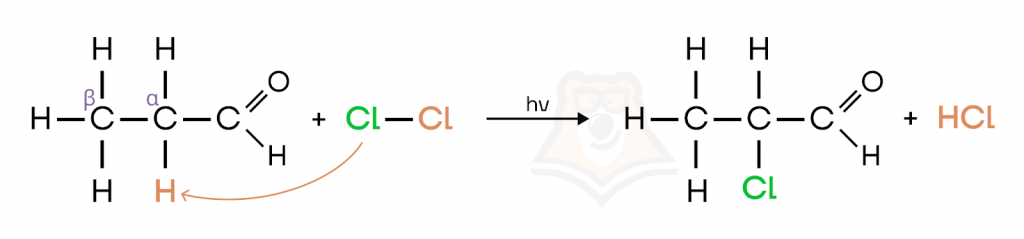
г) Реакции окисления.
- Реакция серебряного зеркала.
Такое название эта реакция получила из-за того, что на стенках колбы или пробирки, в которой проводилась реакция, образуется красивый налет серебра.

Реакция серебряного зеркала — взаимодействие альдегидов с аммиачным раствором оксида серебра (реактив Толленса), в ходе которого образуется аммиачная соль карбоновой кислоты.

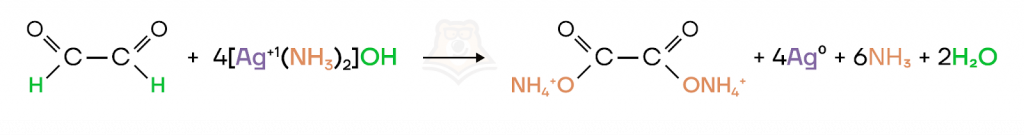
Исключение: формальдегид окисляется до карбоната аммония.
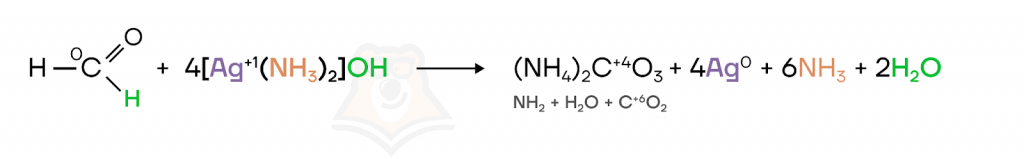

Реакция серебряного зеркала является качественной на альдегиды. Кетоны не вступают в реакцию серебряного зеркала.

- Взаимодействие с гидроксидом меди(II).
В результате реакции выпадает красно-кирпичный осадок оксида меди(I).
Альдегиды, за исключением муравьиного, при этом окисляются до карбоновых кислот. Муравьиный альдегид дает углекислый газ.
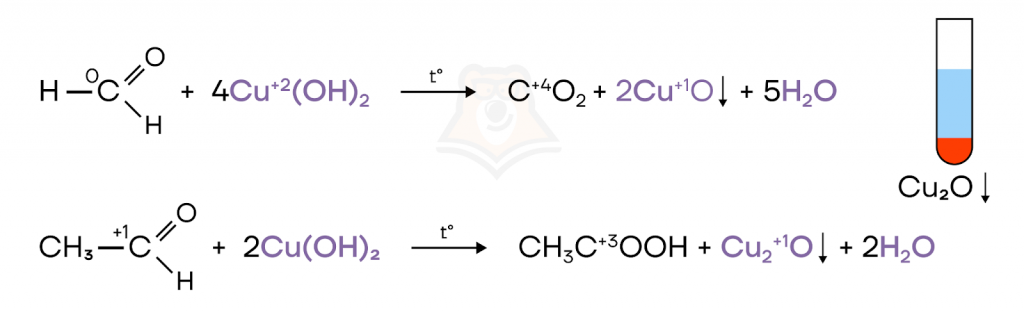


Качественная реакция на альдегиды. Кетоны в эту реакцию не вступают.
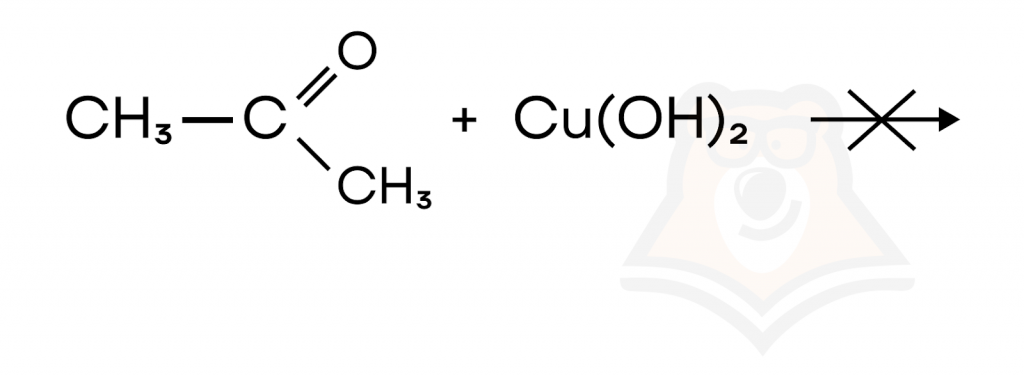
- Жесткое окисление альдегидов.
При окислении перманганатами или хроматами в кислой среде альдегиды превращаются в карбоновые кислоты, в нейтральной или щелочной — в соли карбоновых кислот.
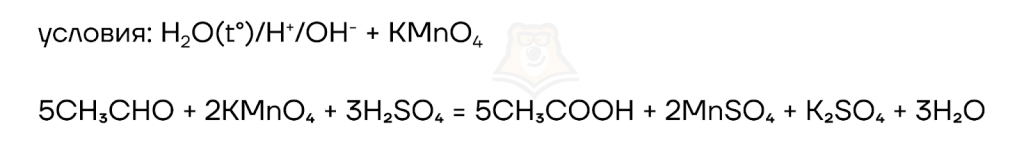

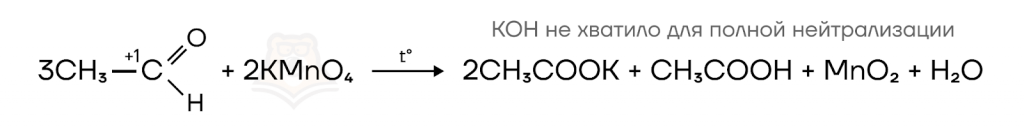
Рассмотрим реакцию окисления этаналя перманганатом калия в нейтральной среде. У этой реакции есть одна особенность. В результате реакции образуется не только соль карбоновой кислоты ацетат калия, но и уксусная кислота. Щелочь, которая образуется в ходе реакции, не может полностью нейтрализовать кислоту до ее соли.
- Горение.
Здесь все просто: все кислородсодержащие соединения сгорают до углекислого газа и воды.

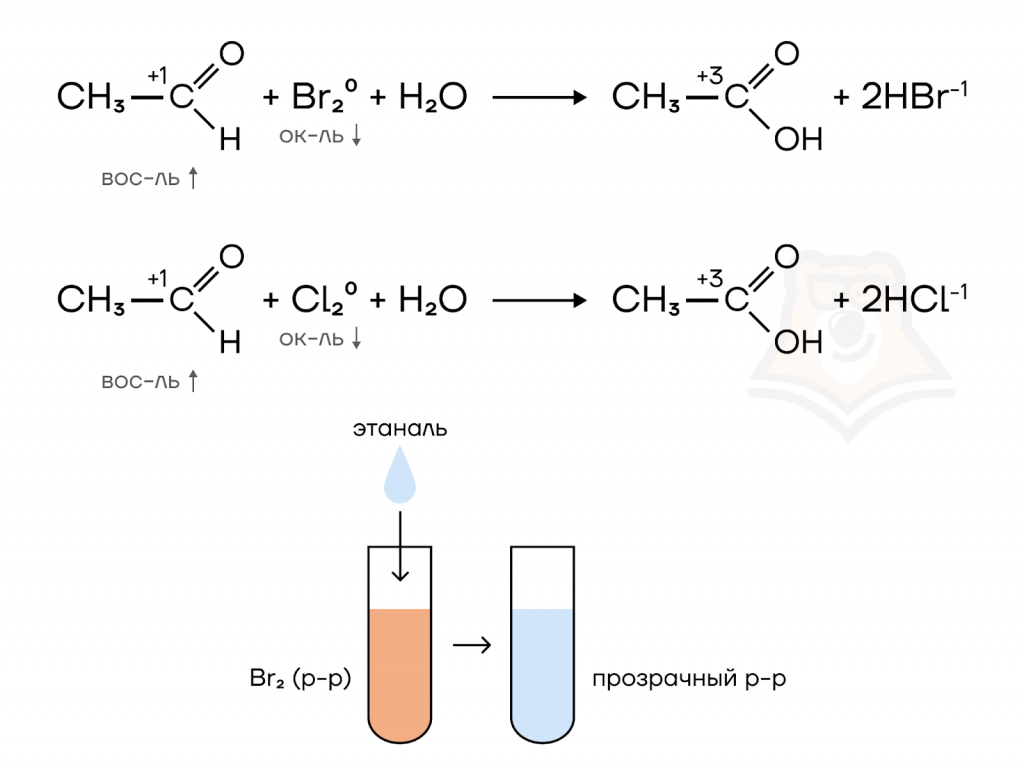
- Окисление хлорной и бромной водой (обесцвечивание).
Хлор и бром, являясь сильными окислителями, могут также окислять альдегиды до карбоновых кислот. При этом в случае с бромной водой происходит обесцвечивание раствора.
Решим задание подобное вопросу № 12 ЕГЭ.
Задание.
Из предложенного перечня выберите формулы всех веществ, которые могут реагировать с этаналем.
1) NaOH
2) Cu(OH)2
3) C2H5OH
4) HBr
5) Cl2
Решение.
1) С гидроксидом натрия этаналь в реакцию не вступает. Ответ не подходит.
2) Реакция с гидроксидом меди(II) — качественная на альдегиды. В результате реакции выпадает осадок оксида меди(I) красно-кирпичного цвета, а этаналь окисляется до уксусной кислоты. Ответ подходит.

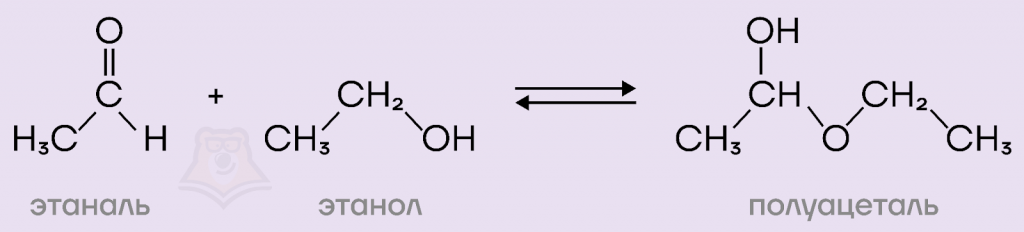
3) При взаимодействии этаналя с этиловым спиртом образуется полуацеталь. Ответ подходит.
4) С бромоводородом альдегиды не взаимодействуют. Ответ не подходит.
5) При взаимодействии с хлором произойдет либо замещение по альфа-атому углерода, либо окисление этаналя до уксусной кислоты. Это будет зависеть от условий проведения реакции. Но для нас в этом задании важен факт того, что вещества взаимодействовать будут.
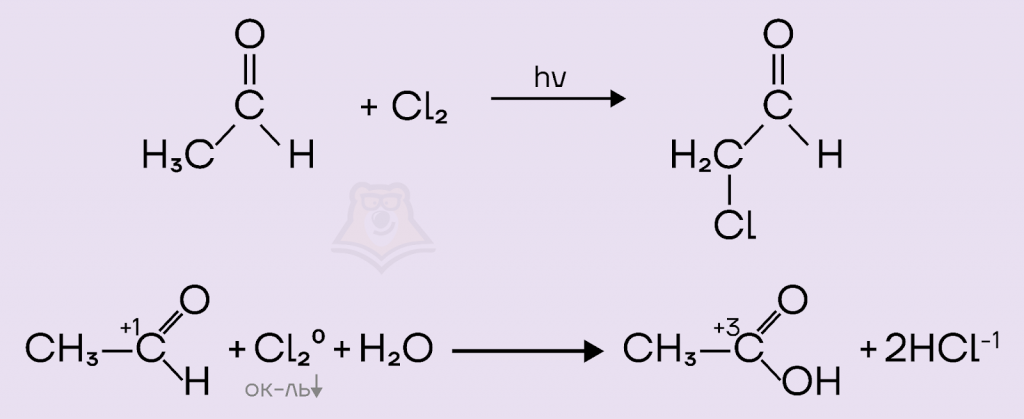
Ответ подходит.
Ответ: 235
Рассмотрим способы получения альдегидов и кетонов.
Получение альдегидов и кетонов
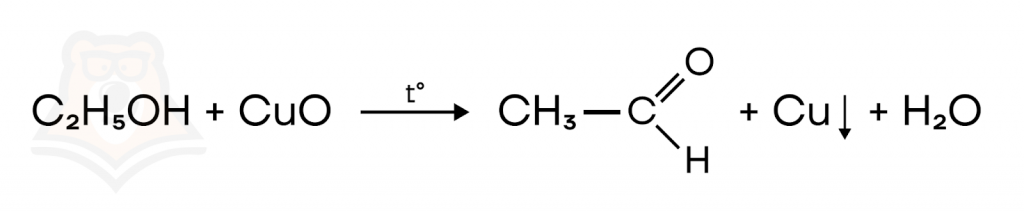
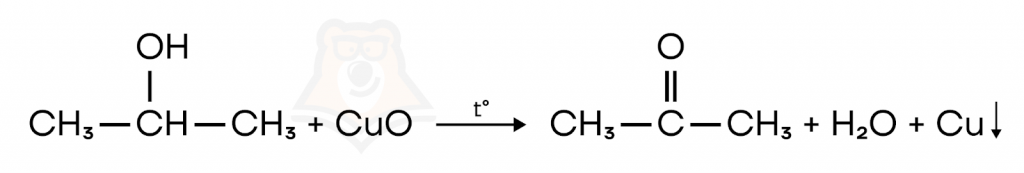
- Мягкое окисление спиртов оксидом меди(II).
Первичные спирты окисляются до альдегидов, вторичные — до кетонов.
- Дегидрирование спиртов.
При пропускании спиртов через медь образуются карбонильные соединения. Из первичных спиртов образуются альдегиды, из вторичных — кетоны. Вспомнить классификацию спиртов можно перейдя в статью «Предельные одноатомные и многоатомные спирты, фенол».
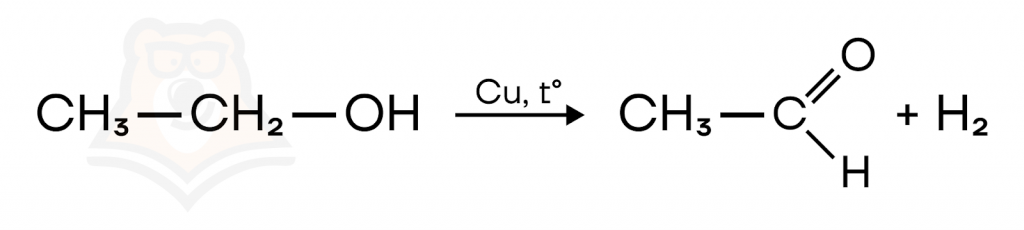
- Каталитическое окисление алкенов.
При окислении этилена кислородом в присутствии катализаторов образуется этаналь, пропена — ацетон.
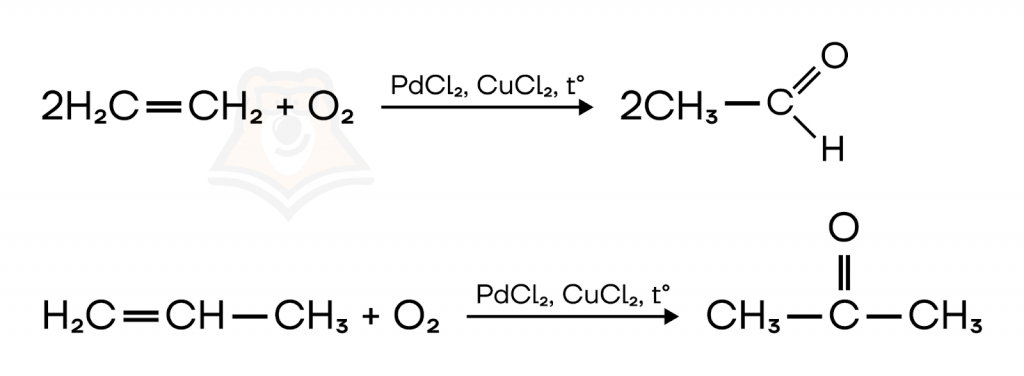
- Щелочной гидролиз дигалогенпроизводных.
Если атомы галогена находятся у одного атома углерода, то щелочный гидролиз таких галогенпроизводных приводит к образованию геминальных диолов, которые из-за своей неустойчивости быстро теряют воду и превращаются в альдегиды или кетоны.
Если галогены расположены у крайнего атома углерода, то образуются альдегиды, если у вторичного атома углерода — образуются кетоны.
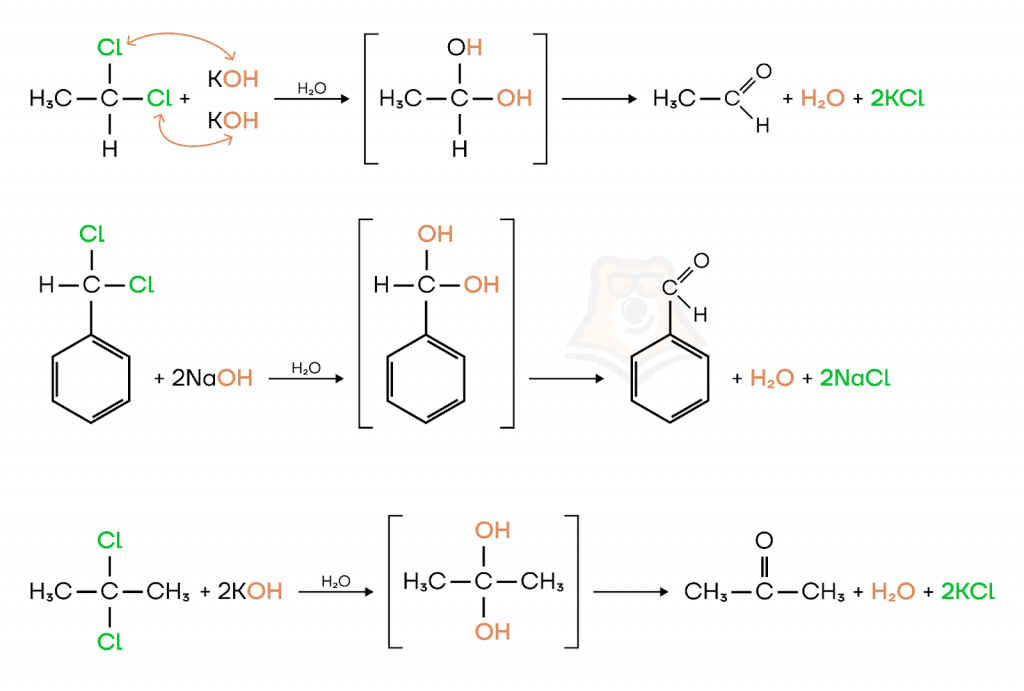
- Термическое разложение кальциевых и бариевых солей карбоновых кислот.
Соли карбоновых кислот двухвалентных металлов при нагревании распадаются на кетон и неорганическую соль.
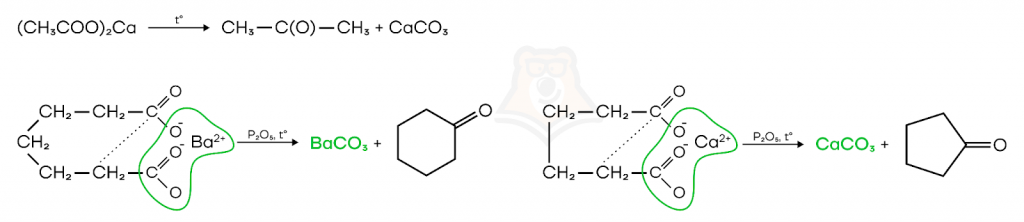
- Кумольный метод.
Ацетон в промышленности получают каталитическим окислением кумола.
Первый этап: получение кумола реакцией алкилирования бензола пропеном.
Реакция алкилирования представляет собой добавление в структуру исходного соединения алкильных заместителей.
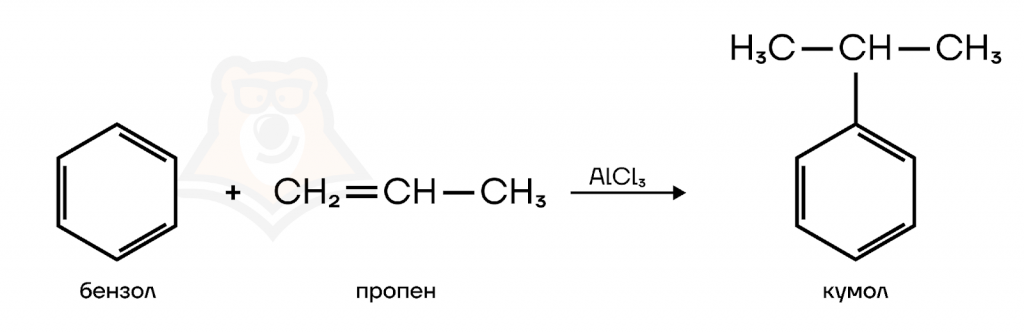
Второй этап: окисление кумола кислородом.

- Реакция Кучерова — присоединение воды к алкинам.
Гидратация ацетилена является промышленным способом получения уксусного альдегида. Только из ацетилена можно получить альдегид этаналь.

Из других алкинов получают кетоны. Например, из пропина получают ацетон.

- Каталитическое окисление метана.
В результате реакции образуется метаналь.

Решим задание, подобное вопросу №14 ЕГЭ.
Задание.
Установите соответствие между органическим соединением и продуктом, который преимущественно образуется при его взаимодействии с водой.
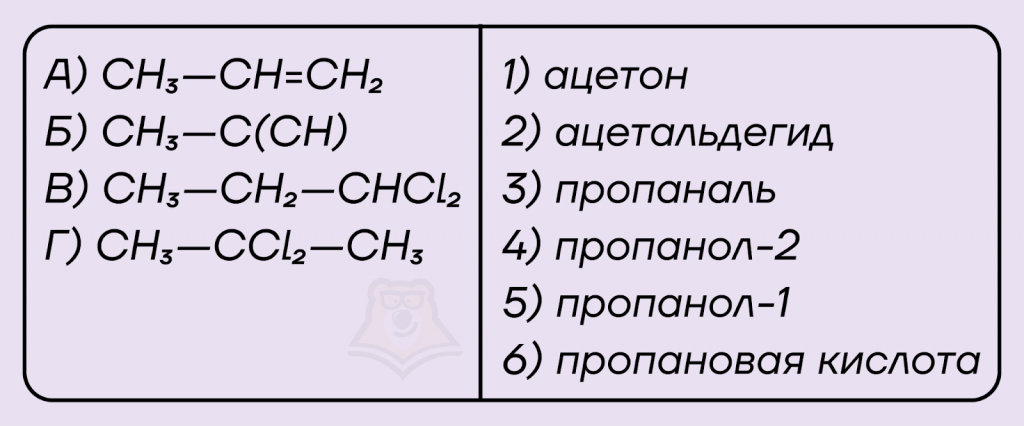
Решение.
Вспоминаем химические свойства.
При взаимодействии пропена (А) с водой образуется спирт пропанол-2. Реакция протекает по правилу Марковникова.
Ответ 4.

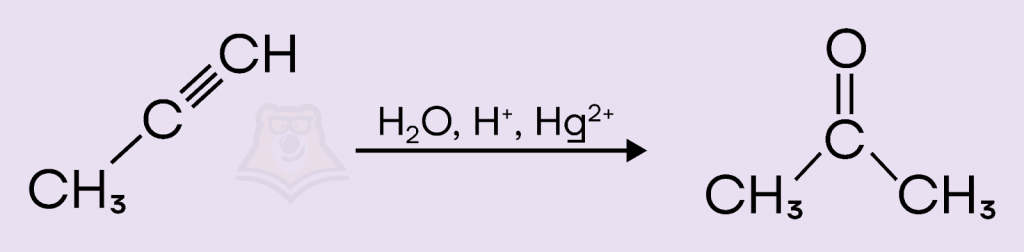
При взаимодействии пропина (Б) с водой образуется ацетон (диметилкетон). Это реакция Кучерова. Важно помнить, что реакция протекает в кислой среде, в качестве катализатора в данной реакции используют ионы ртути. Ответ 1.
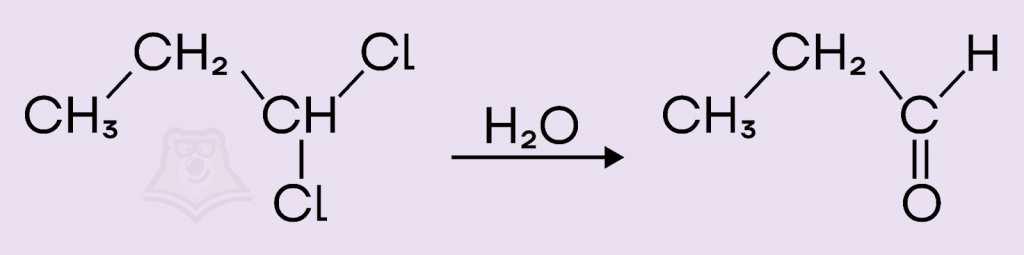
Взаимодействие хлоралкана 1,1-дихлорпропана (В) с водой приведет к образованию альдегида пропаналя. В данной реакции образование альдегида обусловлено расположением атомов галогенов в цепи исходного соединения. Они находятся в первом положении. Ответ 3.
Если же атомы галогена будут расположены у второго атома в цепи галогеналкана, как в примере (Г), то образуется кетон — ацетон. Ответ 1.
Ответ: 4131
Следующий важный раздел, который нам необходимо рассмотреть — применение альдегидов и кетонов.
Применение альдегидов и кетонов
Альдегиды и кетоны — это органические соединения, которые играют важную роль во множестве химических реакций и биологических процессов.
Карбонильные соединения нашли широкое применение в нашей жизни. Ацетон активно используется как растворитель, вспомним жидкость для снятия лака с ногтей. Формальдегид используется для получения фенолформальдегидной смолы, которую, в свою очередь, используют в производстве пластмасс, лакокрасочных, композитных, изоляционных материалов. Раствор формальдегида в воде — формалин — используется для хранения биологических препаратов за счет его способности останавливать процессы разложения.
| Что хранят в формалине? Благодаря свойству формалина свертывать абсолютно все белки, его используют для приготовления влажных препаратов, в которых живые организмы могут не разлагаться много десятков лет. В формалине хранятся необычные экспонаты в Санкт-Петербургской Кунсткамере, а в Биологическом музее г. Москвы «законсервированы» ценные для науки экземпляры рептилий и амфибий, овощей и фруктов времен Мичуринской биологии, демонстрирующие историю селекции. |
Альдегиды используются как ароматизаторы в производстве парфюмерии, косметических средств. Выше мы уже рассказали подробнее об этой области применения этих органических соединений.
Бензофенон (С6Н5)2С=О способен поглощать УФ-лучи, поэтому применяется в изготовлении кремов для защиты от солнца.
Бензальдегид (C6H5CHO) добавляется даже в выпечку, все из-за его приятного миндального запаха.
Фенолформальдегидная смола очень широко используется для производства пластмасс, из которых изготавливают клеи, сувениры, бижутерию, детали для настольных игр, например, шахмат, шашек, бильярда, ступени эскалаторов, ручки для сковородок, отверток, ножей, чайников, корпусы телефонов и многое другое.
Альдегиды и кетоны широко используются во многих отраслях промышленности и научных исследований. Они являются важными предшественниками в синтезе органических соединений, в том числе для синтеза уксусной кислоты, спиртов, лекарственных препаратов.
Кроме того, альдегиды и кетоны являются ключевыми участниками в реакциях окисления и превращениях в рамках метаболических путей в живых организмах. Они участвуют в образовании энергии, метаболизме углеводов и жирных кислот, а также в процессах детоксикации и сигнальных механизмах.
Если вы интересуетесь органической химией и хотите расширить свои знания о важном классе органических соединений, то статья «Карбоновые кислоты» ждет вас.
Термины
Алифатические углеводороды — группа нециклических по структуре углеводородного скелета органических соединений, состоящих только из атомов углерода и водорода.
Алкильный радикал — это функциональная группа органического химического вещества, которая содержит только атомы углерода и водорода, которые расположены в цепи. Они имеют общую формулу CnH2n+1. Примеры включают метил CH3 (производное от метана) и бутил C2H5 (производное от бутана).
Катализатор — вещество, ускоряющее химическую реакцию, но не расходующееся в ней.
Электронная плотность — плотность вероятности обнаружения электрона в данной точке конфигурационного пространства.
Фактчек
- Альдегиды и кетоны — органические соединения, которые содержат одну и ту же функциональную карбонильную группу, но различаются расположением карбонильной группы в углеводородном скелете молекулы.
- Общая формула альдегидов и кетонов одинаковая и выглядит так: СnH2nО
- Гомологами альдегидов и кетонов будут альдегиды и кетоны, которые имеют такое же расположение карбонильной группы, но отличаются на одну или несколько -CH2-групп.
- Для альдегидов и кетонов выделяют три вида изомерии: изомерию углеродного скелета, положения оксогруппы и межклассовую изомерию.
- Альдегиды — химически более активные соединения, чем кетоны. Это объясняется строением этих соединений и электронными эффектами алкильных заместителей.
Проверь себя
Задание 1.
Какое из представленных соединений является кетоном?
- Пропанол
- Пропанон
- Пропан
- 2-хлорпропаналь-1
Задание 2.
С каким соединением вступают в реакцию альдегиды?
- Серной кислотой
- Гидроксидом меди(II)
- Гидроксидом магния
- Диметиловым эфиром
Задание 3.
С чем не взаимодействуют кетоны?
- Водородом
- Синильной кислотой
- Фосфорной кислотой
- Кислородом
Задание 4.
Какая из приведенных ниже реакций является качественной на альдегиды?
- Кучерова
- Гидрирования
- Поликонденсации
- Серебряного зеркала
Задание 5.
Какой основной органический продукт образуется в результате реакции жесткого окисления этаналя в кислой среде?
- Этановая кислота
- Муравьиная кислота
- Формиат калия
- Ацетат калия
Ответы: 1. — 2; 2. — 2; 3. — 3; 4. — 4; 5. — 1.

 к списку статей
к списку статей