
На этой странице вы узнаете
- На что похож клубок шерстяных ниток?
- Какая такая денатурация происходит при готовке?
- Сахар может быть полезным для химиков?
Мы можем даже не замечать, но каждый день мы едим сотни белков, жиров и углеводов. Эти вещества выполняют важные функции в нашем организме. Белки необходимы для роста и развития организма. Жиры необходимы для построения многих тканей в организме человека и являются резервным источником энергии для нас. Углеводы являются топливом биохимический машины, называемой «человек». Но все ли мы знаем о биологически важных веществах? В этой статье речь пойдет о белках и углеводах. А вот о жирах вы можете почитать в статье «Сложные эфиры и жиры».
Белки
Белки (протеины) — это биологически активные вещества, которые состоят только из альфа-аминокислот, связанных пептидной связью.
Кроме обычных или простых белков (протеинов) выделяют и сложные белки (протеиды). Протеиды в отличие от протеинов содержат неаминоксилотные фрагменты — простетические группы, например остатки жиров, углеводов или атомы металлов.
Давайте рассмотрим общее строение белков.
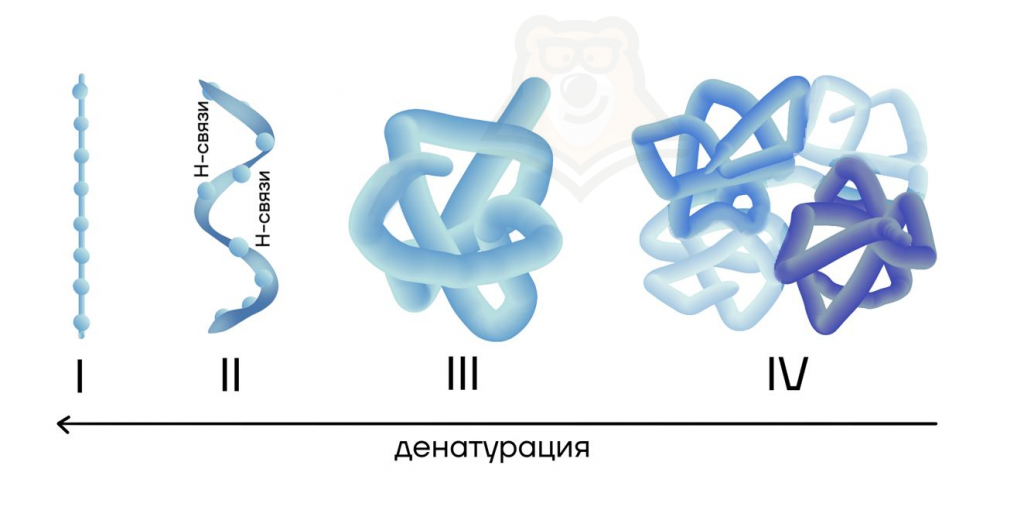
Всего выделяют четыре пространственные структуры белка:
- I — первичная структура. Под первичной структурой понимают последовательность аминокислот в молекуле белка.
- II — вторичная структура. Вторичная структура — спиральная форма, формирующаяся за счет образования водородных связей между N-H и C=O группами.
- III — третичная структура. Клубок, в который закручивается спираль за счет водородных связей, S-S связей между остатками серосодержащих аминокислот и межмолекулярных взаимодействий, называют третичной структурой белка.
- IV — четвертичная структура. При взаимодействии нескольких белковых молекул образуется четвертичная структура белка — большие белковые комплексы.
| На что похож клубок шерстяных ниток? Можно представить, что третичная структура — это клубок шерстяных красных ниток бабушки, которая вяжет однотонный свитер. Тогда четвертичная структура — более крупный клубок из ниток разных цветов. |

Химические свойства белков
К счастью, белки — простые ребята, и нам не надо знать так уж много об их свойствах. Всего три пункта на запоминание.
- Гидролиз
Белки подвержены гидролизу, причем может протекать как полный гидролиз (с образованием набора исходных аминокислот или их солей), так и частичный (с образованием полипептидов меньшего размера).
Гидролиз — один из способов анализа белка, позволяющий установить, какие аминокислоты и в каком количестве входят в его состав. Однако, таким способом нельзя установить, в какой последовательности аминокислоты располагались в белке.
В присутствии кислоты гидролиз протекает с образованием солей по аминогруппе, поскольку аминогруппа обладает основными свойствами.
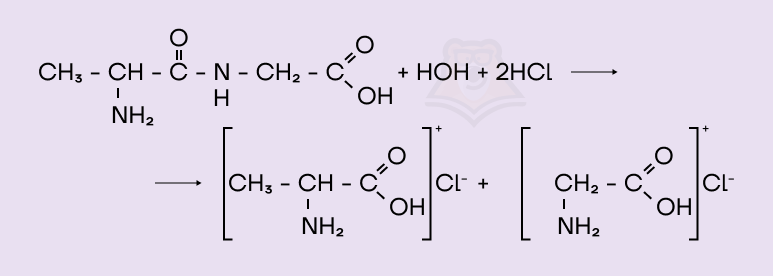
В щелочной среде проявляются кислотные свойства карбоксильных групп аминокислот, так что гидролиз сопровождается образованием солей по карбоксильной группе.
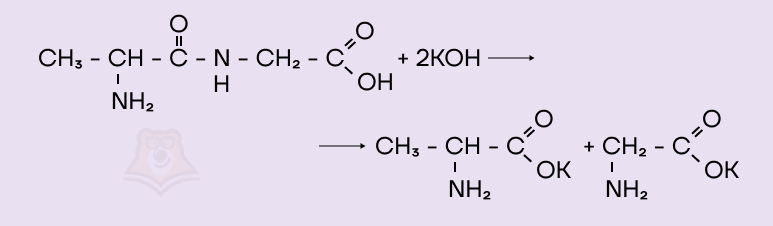
- Денатурация
Денатурация — процесс разрушения белка под действием внешних факторов.
Различают обратимую и необратимую денатурацию. В ходе обратимой денатурации первичная структура белка сохраняется, при устранении внешнего воздействия белок восстановится. Необратимая денатурация сопровождается нарушением первичной структуры белка.
Денатурация может быть вызвана различными факторами.
- Физические:
— высокая температура;
— УФ-излучение;
— радиоактивное излучение;
— механическое воздействие. - Химические:
— действие кислот и щелочей;
— действие ионов тяжелых металлов;
— действие органических растворителей.
| Какая такая денатурация происходит при готовке? Когда мы варим яйцо (белок), оно меняет свою структуру: из жидкого состояния переходит в более плотное в зависимости от того, как долго мы оставляем яйцо вариться. Это и называется денатурацией белка: изменение структуры молекулы белка под воздействием дестабилизирующего фактора (высокой температуры). |

- Цветные (качественные) реакции
Для количественного определения белков используют так называемые «цветные реакции». В ходе этих реакций мы можем наблюдать ярко выраженные видимые признаки.
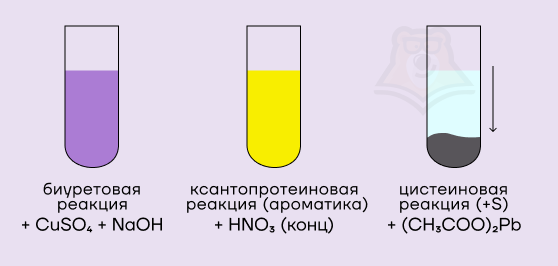
- Биуретовая реакция
Взаимодействие белков со свежеосажденным гидроксидом меди(II) в присутствии щелочи приводит к образованию комплексных соединений, окрашивающих пробу в сине-фиолетовый цвет.
- Ксантопротеиновая реакция
Концентрированная азотная кислота способна «проявить» ароматические аминокислоты в составе белка. В присутвии азотной кислоты ароматические фрагменты нитруются и придают пробе желтую окраску.
- Цистеиновая реакция
Цистеиновая реакция показывает наличие серосодержащих аминокислот в белке. Реакция протекает под действием ацетата свинца(II) и сопровождается образованием черного осадка сульфида свинца(II).
Получение белков
Получение белков чисто химическим путем — задача непростая, и так можно получать лишь относительно небольшие белковые молекулы. Получение не только поли-, но и даже олигопептидов происходит в результате трудоемкого многостадийного органического синтеза.
Для общего представления об этом процессе нам пока достаточно знать, что при взаимодействии двух ⍺-аминокислот происходит образование дипептида.
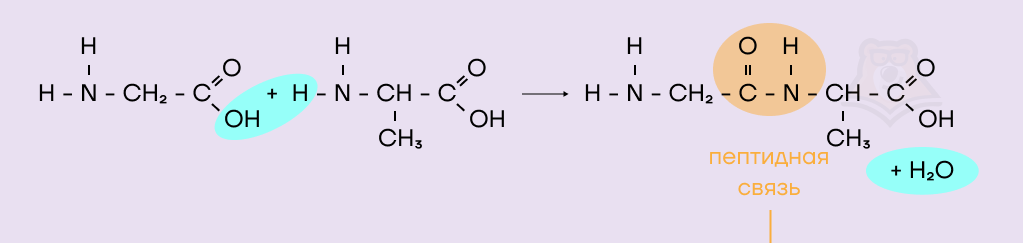
Образовавшийся дипептид также имеет амино- и карбоксильную группу и может вступать в реакцию с другими аминокислотами с образованием пептидной связи. Так постепенно можно получить достаточно сложную полипептидную молекулу.
Основным же способом синтеза белка является биосинтез, в этом процессе необходимые белки «выращивают» в живых организмах.
С белками разобрались, теперь переходим к углеводам.
Углеводы
Углеводы — это органические вещества, которые содержат одну карбонильную и несколько гидроксильных групп. Состав большинства углеводов может быть выражен как Cn(H2O)n.
Углеводы широко распространенные и важные органические соединения, они выполняют важные функции в живых организмах. Структурная и опорная функции — из углеводов построены клеточные стенки грибов и растений, а также экзоскелеты насекомых. Запасающая и энергетическая — животные запасают энергию с помощью углевода гликогена, растения с помощью крахмала; с другой стороны при окислении углеводов в ходе метаболизма высвобождается значительное количество энергии, позволяющее поддерживать жизнедеятельность организма.
Кроме важной биологической роли углеводов стоит отметить и их значение для хозяйственной деятельности человека. Углеводы находят применение в пищевой, текстильной, фармацевтической, целлюлозно-бумажной и химической промышленности.
Основным способом классификации углеводов является классификация по количеству структурных звеньев в молекуле:
- моносахариды — углеводы, содержащие одно структурное звено;
- олигосахариды содержат от двух до 10 структурных звеньев;
- полисахариды могут содержать до нескольких тысяч структурных звеньев.
Моносахариды
Моносахариды, в свою очередь, можно разделить на несколько классов.
Один из способов классификации делит моносахариды на основании типа карбонильной группы, которая входит в их состав:
- альдозы содержат альдегидную группу;
- кетозы содержат кетонную группу.
Еще одним способом классификации углеводов является классификация по количеству атомов углерода в составе молекулы углевода, здесь выделяют:
- триозы содержат 3 атома углерода;
- тетрозы содержат 4 атома углерода;
- пентозы содержат 5 атомов углерода;
- гексозы содержат 6 атомов углерода.
Два указанных способа классификации независимы и могут быть объединены, так что классифицировать моносахариды можно сразу по двум признакам.
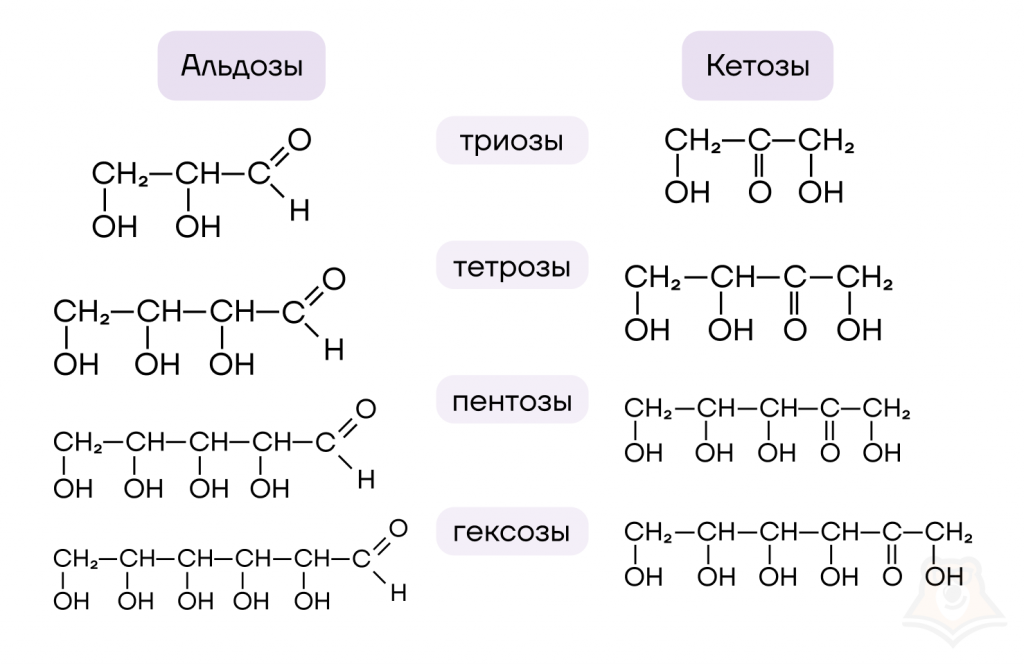
Стоит запомнить строение и названия некоторых важнейших моносахаридов.
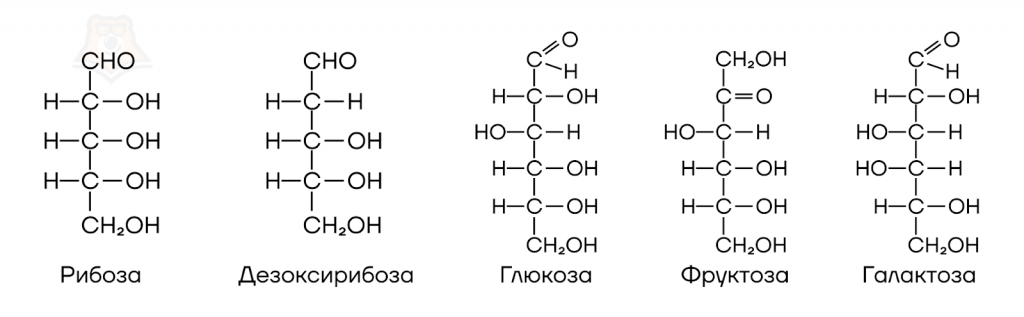
Что касается физических свойств моносахаридов, то все они сладкие на вкус, белые и хорошо растворимы в воде (за счет возможности образования водородных связей между молекулами углеводов и воды).
Кольчато-цепная таутомерия
Таутомерия — тип изомерии, особенностью которого является легкость превращения изомеров друг в друга.
Молекулы моносахаридов содержат карбонильную и гидроксильные группы, то есть являются одновременно альдегидами/кетонами и многоатомными спиртами.
Стоит помнить, что карбонильные соединения способны реагировать со спиртами с образовазованием полуацеталей/полукеталей. В случае моносахаридов возможно внутримолекулярное взаимодействие между карбонильной и гидроксильной группами, приводящее к образованию их циклической формы. Таким образом, существует равновесие между цепной и кольчатой формой моносахаридов.
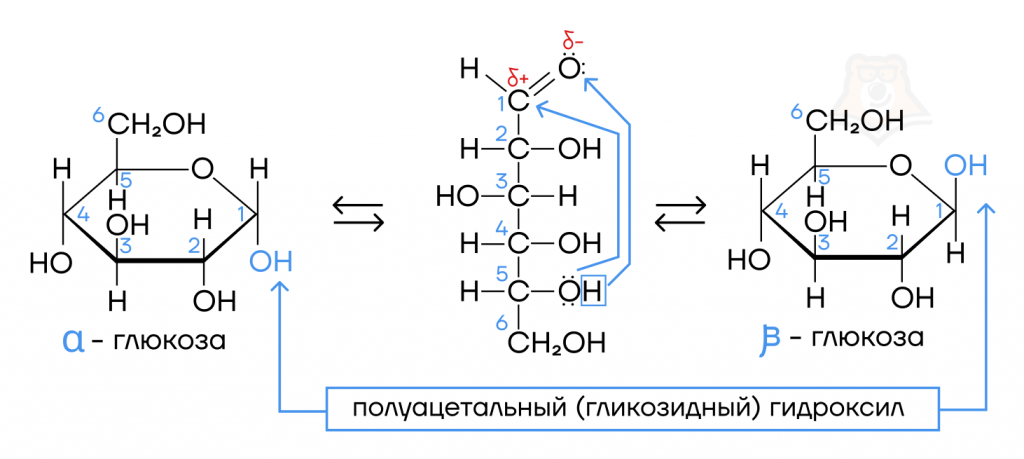
Химические свойства моносахаридов
Теперь перейдем к химическим свойствам моносахаридов. Рассмотрим их на примере глюкозы, которая имеет альдегидную группу, за счет чего для нее характерны реакции альдегидов.
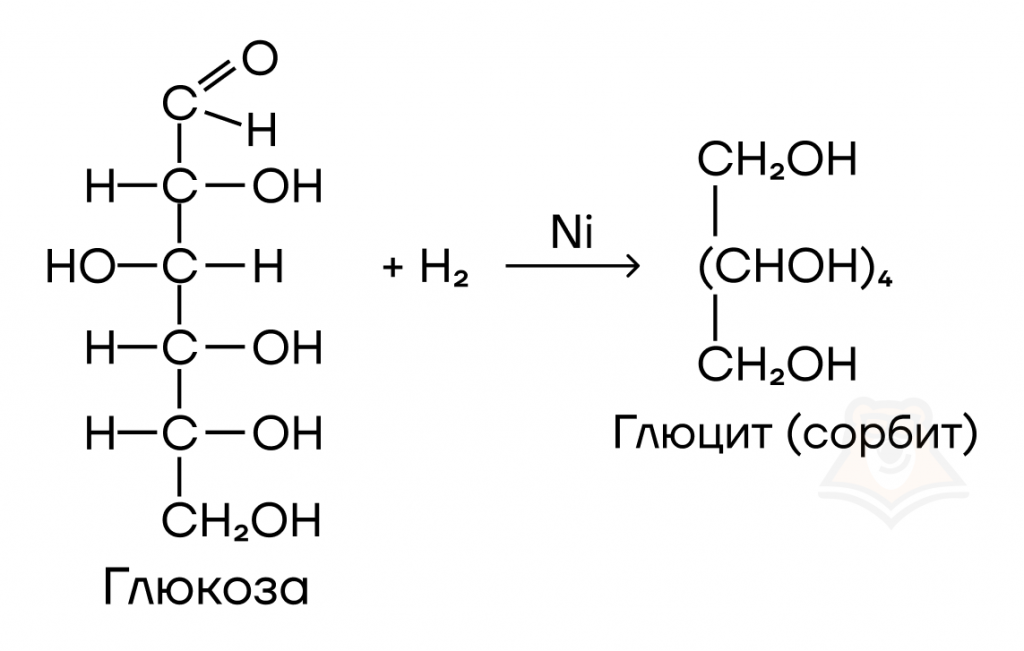
- Каталитическое гидрирование, сопровождающееся образованием многоатомного спирта — сорбита, который используется в качестве сахарозаменителя.
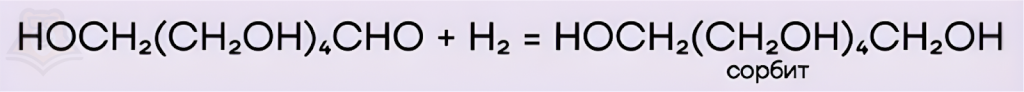
- Окисление. В ходе реакций окисления альдегидная группа окисляется до карбоксильной, в нейтральной и кислой среде образуется глюконовая кислота, в щелочной — ее соли. Для альдоз характерны несколько различных реакций окисления:
- реакция серебряного зеркала;
- взаимодействие со свежеосажденным гидроксидом меди(II);
- взаимодействие с другими окислителями, такими как перманганат калия.
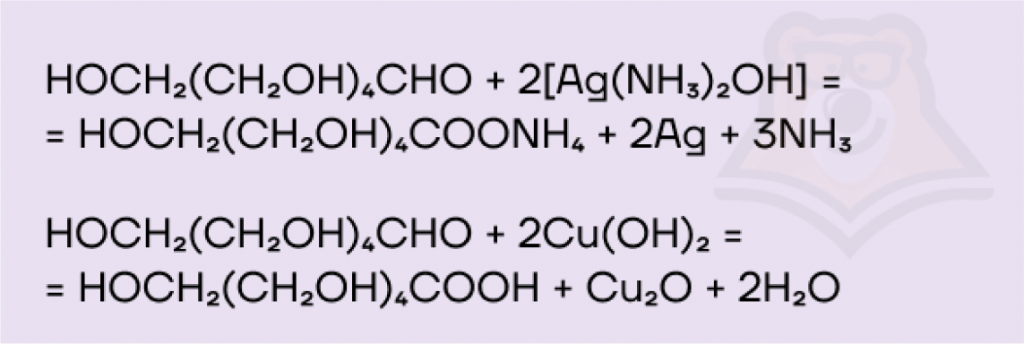
Все моносахариды имеют свойства многоатомных спиртов, так как содержат несколько гидроксильных групп. С ними можно ознакомиться в статье «Предельные одноатомные и многоатомные спирты, фенол».
Наиболее важным свойством, которое досталось глюкозе от многоатомных спиртов, является качественная реакция с гидроксидом меди(II). Как многоатомный спирт при взаимодействии со свежеосажденным гидроксидом меди(II) глюкоза образует комплексное соединение, придающее раствору синее окрашивание.
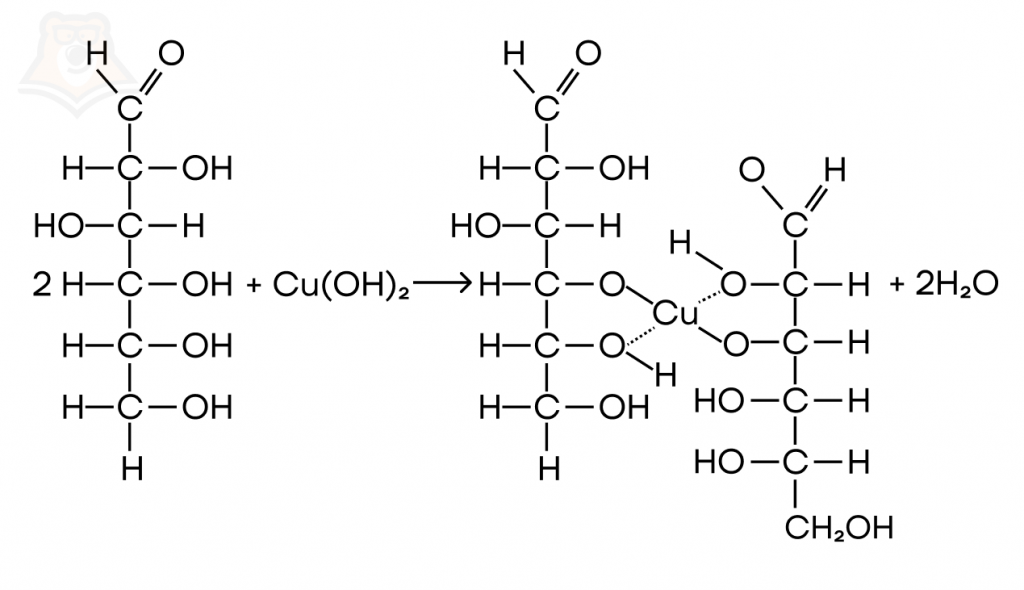
При нагревании полученного раствора синяя окраска постепенно ослабевает и образуется кирпично-красный осадок оксида меди(I), что связано с протеканием реакции окисления альдегидной группы, о которой говорилось выше.
А также у глюкозы есть особые свойства: брожение нескольких видов. Именно это свойство используют в производстве разных напитков, например, пива и кефира.
Различают следующие виды брожения.
- Спиртовое брожение — процесс, сопровождающийся образованием этилового спирта.
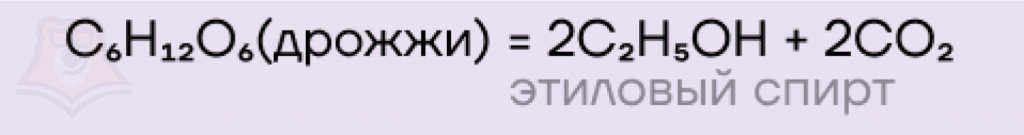
- Молочнокислое брожение, как очевидно следует из названия, приводит к образованию молочной кислоты.
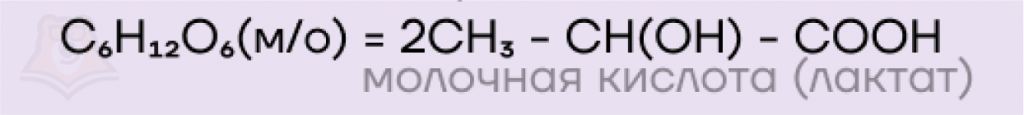
- Маслянокислое брожение, аналогично, приводит к образованию масляной (бутановой) кислоты.
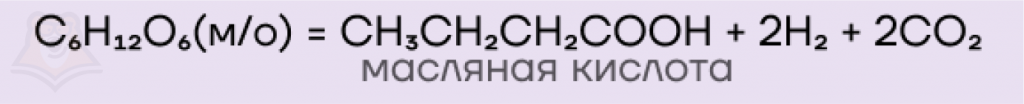
- Лимоннокислое брожение же сопровождается образованием лимонной кислоты.
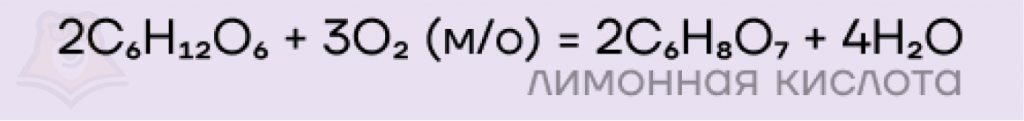
Теперь давайте рассмотрим свойства моносахаридов, которые содержат кетогруппу, например, свойства фруктозы.
Наличие кетонной группы обуславливает возможность каталитического гидрирования, приводящего, как и в случае с глюкозой, к образованию сорбита.
Для кетоз, в отличие от альдоз, не характерны реакции окисления, но все еще характерны свойства многоатомных спиртов. Все так же наиболее важной является реакция с гидроксидом меди(II), качественным признаком которой является синее окрашивание пробы.
С чем реагирует глюкоза мы поняли, а как она образуется?
- Фотосинтез — удивительный процесс образования органического вещества — глюкозы, из неорганических — углекислого газа и воды, протекающий в зеленых частях растений. Энергию для протекания этого процесса растения получают от солнца, благодаря зеленому пигменту — хлорофиллу, улавливающему солнечные лучи.
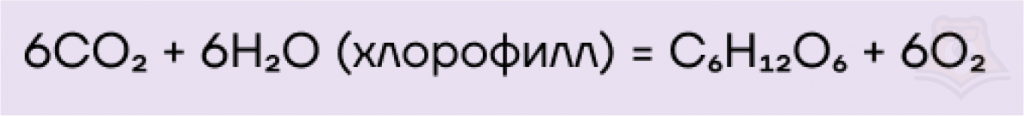
- Гидролиз крахмала и целлюлозы.
Часть глюкозы, образующейся в растениях в ходе фотосинтеза, используется ими для синтеза полисахаридов: крахмала (выполняющего запасающую функцию) и целлюлозы (из которой построены клеточные стенки растений).
Разрушив эти полимеры, можно получить глюкозу обратно. Наиболее удобным способом получения моносахаридов и полисахаридов является их кислый гидролиз.
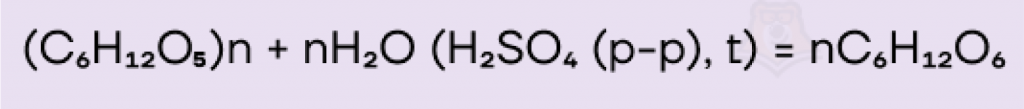
Дисахариды
Дисахариды отличаются от моносахаридов в первую очередь количеством структурных элементов. Молекулы дисахаридов построены из остатков моносахаридов, находящихся в кольчатой форме.
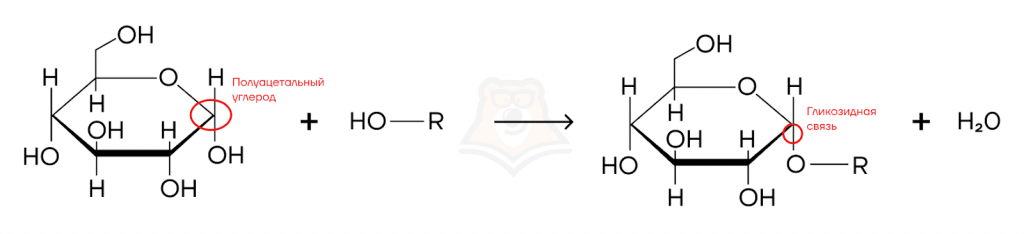
Дисахариды — углеводы, состоящие из двух остатков моносахаридов, связанных гликозидной связью.
Гликозидная связь — связь, образованная между полуацетальной группой углевода и гидроксильным кислородом другого органического соединения, например, другого углевода.
Рассмотрим самых важных представителей дисахаридов.
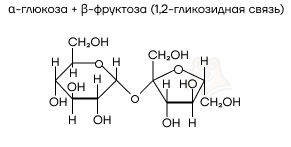
- Сахароза (тростниковый или свекловичный сахар).
- Мальтоза (солодовый сахар).
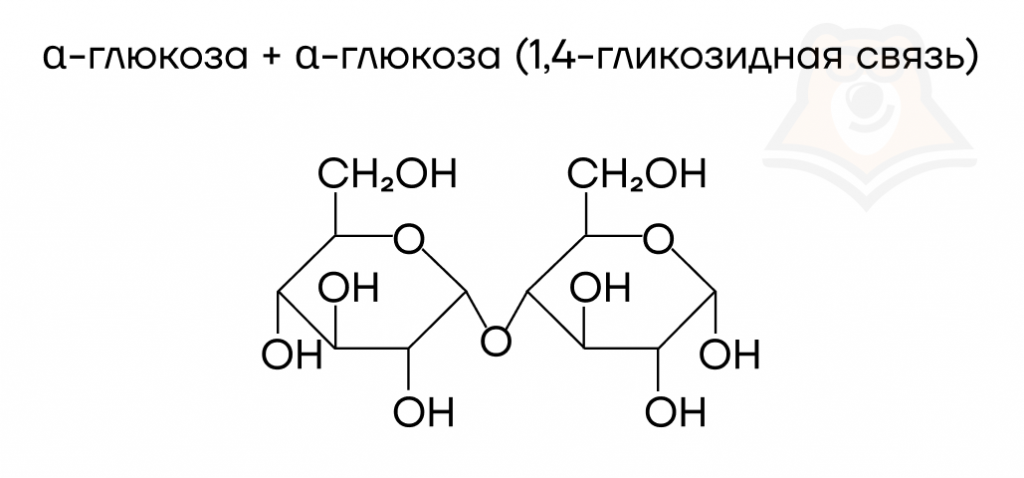
- Лактоза (молочный сахар).
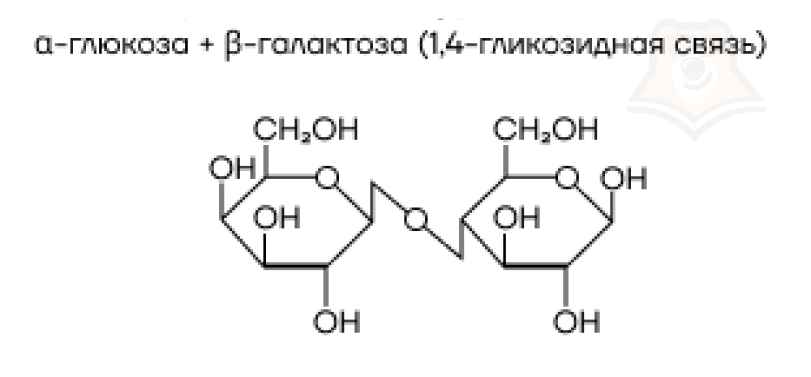
Что касается химических свойств, то дисахариды способны гидролизоваться до мономеров, из которых они образовались:
- сахароза = глюкоза + фруктоза;
- мальтоза = глюкоза + глюкоза;
- лактоза = глюкоза + галактоза.
Полисахариды
К полисахаридам относятся:
- целлюлоза (состоит из бета-глюкозы);
- крахмал (состоит из альфа-глюкозы).
Интересно, что с этими веществами мы достаточно часто встречаемся в повседневной жизни. Например, целлюлозу применяют в производстве лаков, бумаги, пластмасс и твердого ракетного топлива, а крахмал добавляют в пищу, используют в качестве загустителя.
Рассмотрим химические свойства целлюлозы и крахмала.
Химические свойства целлюлозы
- Гидролиз — ферментативный.
В ходе ферментативного гидролиза в молекулах полисахаридов разрушаются гликозидные связи, при этом образуются моносахариды, из которых которых был построен полисахарид. Так при полном гидролизе, например, целлюлозы можно получить 𝛽-глюкозу.
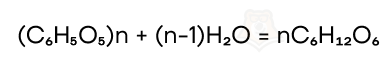
- Взаимодействие с уксусной и азотной кислотой.
В молекулах полисахаридов имеются гидроксильные группы, которые обуславливают возможность образования их сложных эфиров при взаимодействии с кислотами.
При взаимодействии целлюлозы с уксусной кислотой образуется триацетат целлюлозы (ацетилцеллюлоза), который используют для производства кинопленок.
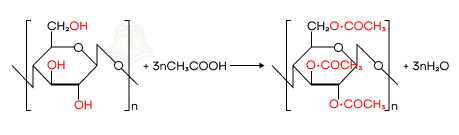
При взаимодействии с азотной кислотой получают нитроцеллюлозу.
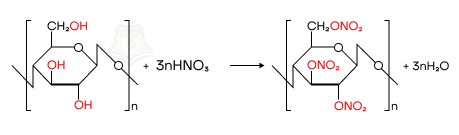
Нитроцеллюлоза — один из первых искусственных полимеров и раньше она широко применялась в производстве различных материалов. Основным недостатком нитроцеллюлозы как материала является то, что она легко воспламеняется, поэтому на данный момент основной областью ее применения является производство бездымного пороха.
Крахмал
Крахмал менее прочен, чем целлюлоза, поэтому он не находит применения в качестве материала и используется главным образом в пищевой промышленности. Еще одно применение крахмала — в качестве клеящего вещества, связано с тем, что при разведении в горячей воде он образует клейстер.
Как и целлюлоза крахмал подвергается гидролизу, при этом образуется 𝛼-глюкоза.
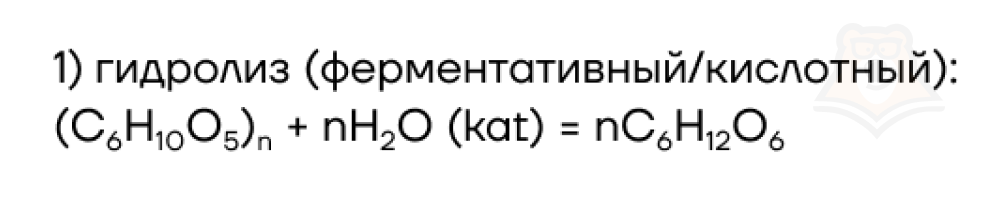
И ди-/олиго-/полисахариды, и белки (к слову, и жиры) подвержены гидролизу, а этот факт может помочь вам в решении задания №13 ЕГЭ по химии. Посмотрим на примере.
Задание. Из предложенного перечня выберите два вещества, которые не вступают в реакцию гидролиза.
1) глюкоза
2) сахароза
3) глицерил стеарат
4) глицин
5) эластин
Решение.
1. Глюкоза — моносахарид — не подвергается гидролизу.
2. Сахароза — дисахарид — подвергается гидролизу.
3. Глицерил стеарат — жир — подвергается гидролизу.
4. Глицин — аминокислота — не подвергается гидролизу.
5. Эластин — белок — подвергается гидролизу.
Ответ: 14
У крахмала есть одно интересное свойство: при взаимодействии с йодом он образует комплексное соединение синего цвета.
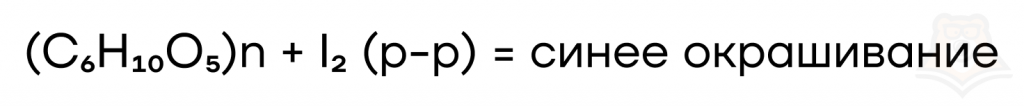
Смесь крахмала с небольшим количеством воды представляет собой неньютоновскую жидкость. Это означает, что такая смесь по-разному ведет себя при столкновении с медленными и быстрыми объектами. Вы легко можете медленно погрузить в нее руку, как в жидкость, но при резком ударе кулаком она становится твердой.
Можете попробовать дома сами!
Сегодня мы познакомились с несколькими качественными реакциями. В ЕГЭ по химии вопросы, касающиеся качественных реакций, представлены в задании №24. Давайте разберем пример.
Задание. Установите соответствие между названиями веществ и реагентом, с помощью которого можно различить эти вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
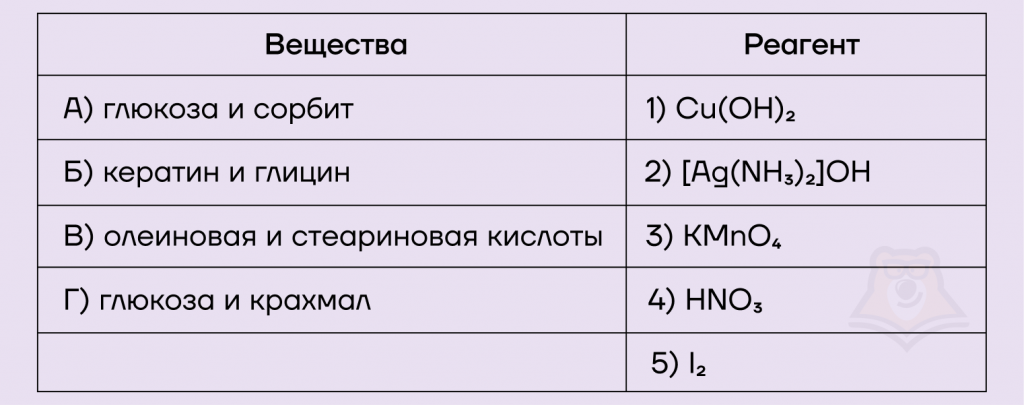
Решение.
А) Глюкоза — альдоза, сорбит — шестиатомный спирт, их можно различить с помощью аммиачного раствора оксида серебра. Ответ — 2.
Б) Кератин — белок, вступает в ксантопротеиновую реакцию, глицин — аминокислота, так что действие на него азотной кислоты не сопровождается видимыми признаками. Ответ — 4.
В) Олеиновая и стеариновая кислоты — высшие жирные кислоты, но олеиновая, в отличие от стеариновой, является непредельной. Непредельные соединения обесцвечивают раствор перманганата калия. Ответ — 3.
Г) Известная качественная реакция на крахмал — взаимодействие с йодом, для глюкозы подобная реакция не протекает. Ответ — 5.
Ответ: 2435
Нуклеиновые кислоты
Нуклеиновые кислоты — ДНК (дезоксирибонуклеиновая кислота) и РНК (рибонуклеиновая кислота) — высокомолекулярные соединения, имеющие исключительную важность для живых организмов, поскольку они ответственны за передачу наследственной информации.
Нуклеиновые кислоты построены из нуклеотидов, которые в свою очередь являются фосфорнокислыми эфирами нуклеозидов, представляющих собой органические соединения, состоящие из связанных между собой азотистого основания и углевода — рибозы или дезоксирибозы.
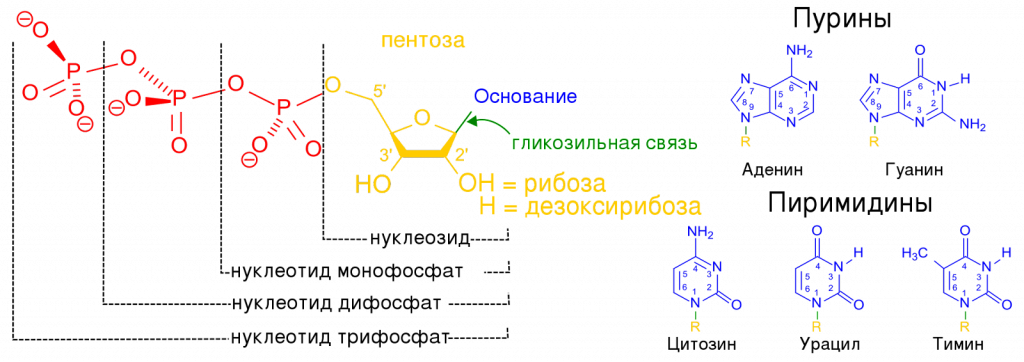
Как и в случае белков, можно выделить 4 уровня организации нуклеиновых кислот:
- первичная структура — последовательность нуклеотидов, соединенных остатками фосфорной кислоты;
- вторичная структура — две цепочки первичной структуры, соединенные между собой водородными связями;
- третичная структура — спиралевидная структура, образующаяся при скручивании двойной цепи за счет образования дополнительных водородных связей;
- четвертичная структура — сложные комплексы нуклеиновых кислот с белками.
На этом рассмотрение белков, углеводов и нуклеиновых кислот подходит к концу. Мы познакомились с их строением и свойствами, качественными реакциями, областями применения и даже узнали пару интересных фактов. Кстати, к концу подошло и рассмотрение важнейших классов органических соединений в принципе, по этому поводу крайне рекомендуется освежить знания, прочитав статью «Генетическая связь между классами органических соединений».
Термины
Дипептид — органическое соединение, состоящее из остатков двух аминокислот, связанных пептидной связью.
Олигопептид — органическое соединение, содержащее от двух до двадцати остатков аминокислот, связанных пептидной связью.
Пептидная связь — разновидность амидной связи, образующаяся при взаимодействия ⍺-аминогруппы одной аминокислоты и ⍺-карбоксильной группы другой.
Фактчек
- Белки — это биологически активные вещества, которые состоят только из альфа-аминокислот.
- Всего выделяют четыре пространственные структуры белка: первичную (последовательность аминокислот), вторичную (спираль), третичную (спираль, свернутую в клубок) и четвертичную (соединение нескольких белковых молекул).
- Белки подвержены гидролизу. При полном гидролизе белка образуется набор аминокислот (или их солей), из которых состоял белок.
- Разрушение структуры белка называют денатурацией.
- Наличие белков в пробе можно определить с помощью цветных реакций: биуретовой, ксантопротеиновой, цистеиновой.
- Углеводы — органические вещества, которые содержат одну карбонильную и несколько гидроксильных групп.
- Углеводы делятся на моносахариды, дисахариды и полисахариды.
- Моносахариды классифицируют двумя способами: по строению функциональной группы и по количеству атомов углерода.
- По строениею функциональной группы выделяют альдозы (содержат альдегидную группу) и кетозы (содержат кетонную группу)
- По количеству атомов углерода выделяют: триозы (3 атома углерода), тетрозы (4 атома углерода) пентозы (5 атомов углерода) и гексозы (6 атомов углерода).
- Все моносахариды сладкие на вкус, белые и хорошо растворимы в воде.
- Для моносахаридов характерны свойства карбонильных соединений и многоатомных спиртов.
- Важнейшим химическим свойством олиго- и полисахаридов является подверженность гидролизу.
- Наличие в пробе крахмала можно определить с помощью йода.
Проверь себя
Задание 1.
К какому из классов соединений относится глюкоза?
- Моносахарид
- Дисахарид
- Полисахарид
- Олигосахарид
Задание 2.
К какому из классов соединений относится фруктоза?
- Протеин
- Углевод
- Жир
- Протеид
Задание 3.
К какому из классов соединений относится крахмал?
- Полисахарид
- Дисахарид
- Олигосахарид
- Белок
Задание 4.
Какое из веществ, названия которых приведены ниже, подвергается гидролизу?
- Глюкоза
- Фруктоза
- Рибоза
- Сахароза
Задание 5.
С помощью какого реагента можно различить глюкозу и фруктозу?
- [Ag(NH3)2]OH
- Cu
- H2
- HCl
Ответы:1. — 1; 2. — 2; 3. — 1; 4. — 4; 5. — 1.

 к списку статей
к списку статей 



