
На этой странице вы узнаете
- Такой ли уж безжизненный азот?
- Азот-хитрец: почему его максимальная валентность не совпадает с высшей степенью окисления?
- Нашатырный спирт — спирт или не спирт?
Азот, наверное, самый удивительный неметалл — он имеет множество степеней окисления и огромное число соединений. И сегодня мы узнаем, каким многогранным он может быть и какие разнообразные свойства проявляют его соединения.
Общая характеристика азота
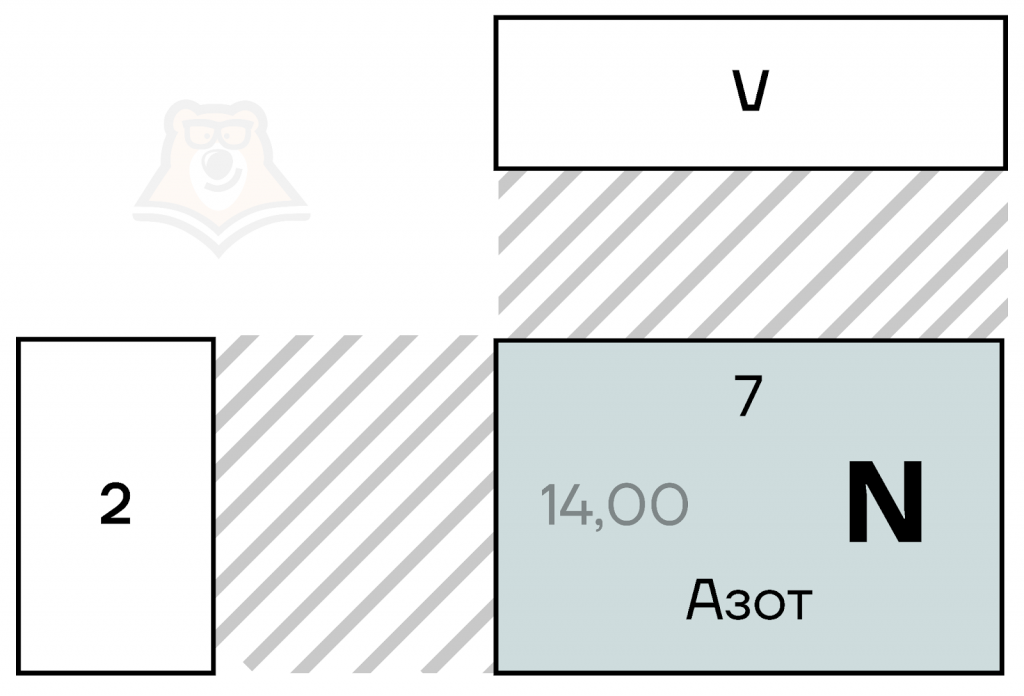
Азот — неметалл с порядковым номером 7, расположен во 2 периоде и входит в состав VA группы, элементы которой называют пниктогенами — «дурно пахнущими».
| Такой ли уж безжизненный? Название элемента «азот» образовано от древнегреческого «ἄζωτος», что буквально переводится как «безжизненный». Тем не менее, азот задействован в образовании пептидных связей между молекулами аминокислот, благодаря которым последние объединяются в белки. Кроме того, азот участвует в целом ряде биохимических процессов: гниении, разложении белков и др. Растениям необходим азот в нитратной форме для роста и развития, а некоторые организмы, такие как клубеньковые бактерии, способны переводить молекулярный азот из атмосферы в аммиачную форму в процессе фиксации азота. |
Рассмотрим электронную конфигурацию внешнего слоя атома азота.
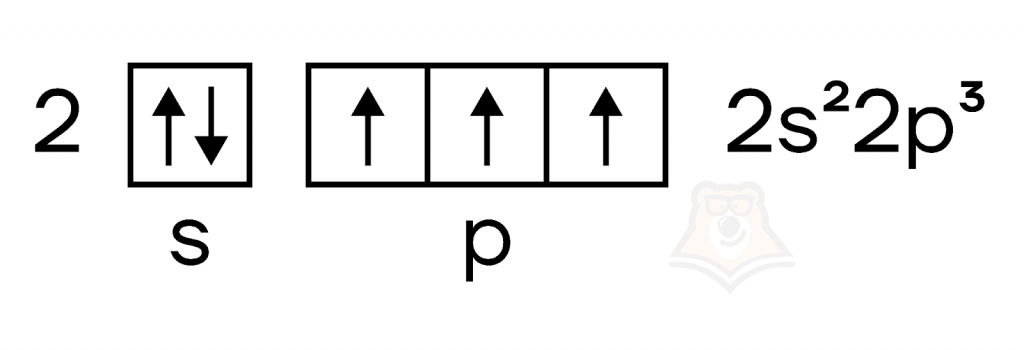
За счет трех неспаренных электронов и электронной пары азот суммарно может образовывать в соединениях 4 химические связи. Это значит, что его максимальная валентность — IV.
Атом азота имеет следующий набор степеней окисления:
- высшая степень окисления равна номеру группы: +5;
- низшая степень окисления определяется по формуле «номер группы — 8»: -3;
- в качестве промежуточных степеней окисления азот может проявлять любые положительные.
Набор степеней окисления азота: -3, 0, +1, +2, +3, +4, +5.
| Азот-хитрец: почему его максимальная валентность не совпадает с высшей степенью окисления? Максимальная степень окисления азота +5, а максимальная валентность — IV. Валентность азота ниже максимальной степени окисления из-за того, что азот образует три связи по обменному механизму (за счет неспаренных электронов), и одну — по донорно-акцепторному (за счет электронной пары). В соединениях азота со степенью окисления +5 реализуются связи, образованные по донорно-акцепторному механизму: |
Получение азота
Существует несколько основных способов получения азота. В промышленности чаще всего азот получают из воздуха в ходе его фракционной перегонки. Воздух охлаждают при повышенном давлении, получая жидкую смесь азота, водорода и других компонентов воздуха, затем полученный жидкий воздух постепенно нагревают. Из жидкости в газ компоненты смеси переходят уже по отдельности в соответствии с температурами их кипения.
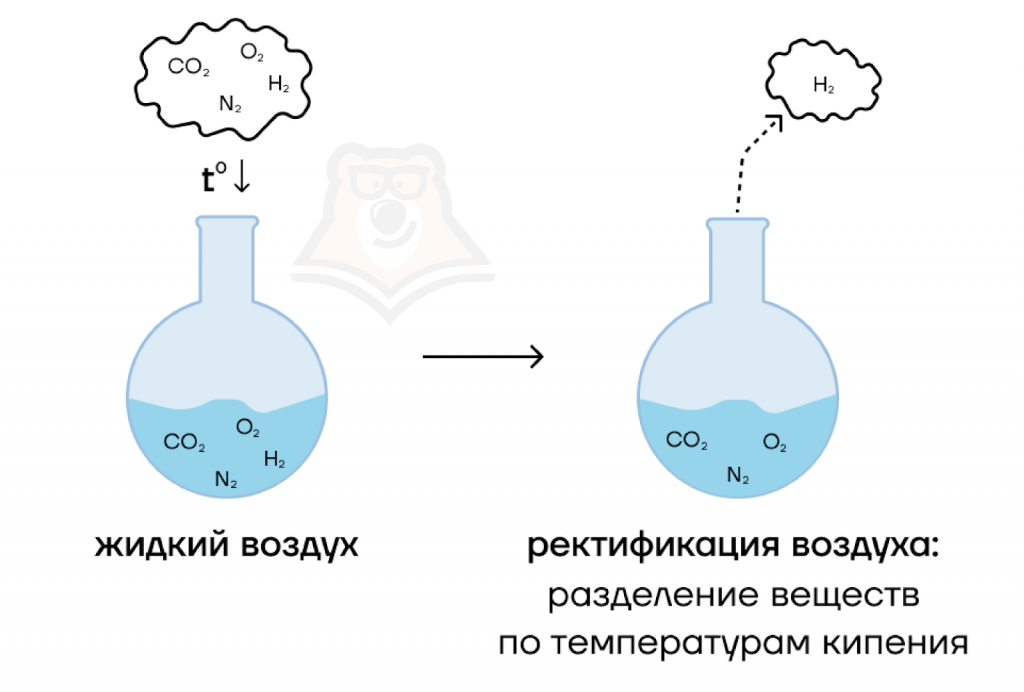
В лаборатории небольшие количества азота можно получить при термическом разложении некоторых соединений.
NH4NO2 = N2 + 2H2O
(NH4)2Cr2O7 = N2 + Cr2O3 + 4H2O
Химические свойства азота
В молекуле азота реализуется тройная связь — между атомами азота в молекуле N2 располагается три общие электронные пары. Разрушить такую связь крайне затруднительно, поэтому азот очень «ленив» — химически неактивен. Для взаимодействия с чем-либо ему нужны будут, как правило, жесткие условия: высокая температура, высокое давление или катализаторы.
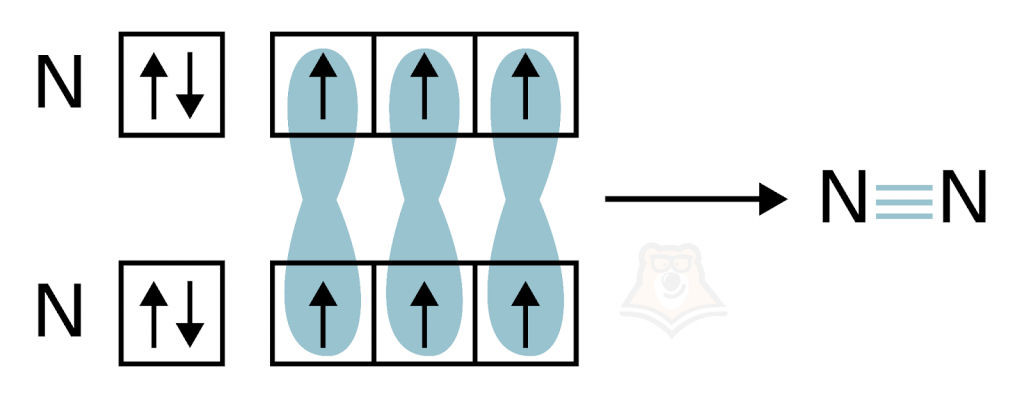
- Взаимодействие с металлами.
️Азот взаимодействует с активными металлами: металлами IA- и IIA-групп, а также с алюминием. В данных реакциях азот проявляет свои окислительные свойства. В результате реакции образуются нитриды. При обычных условиях реакция протекает только с литием и магнием, для взаимодействия с остальными металлами требуется повышенная температура.
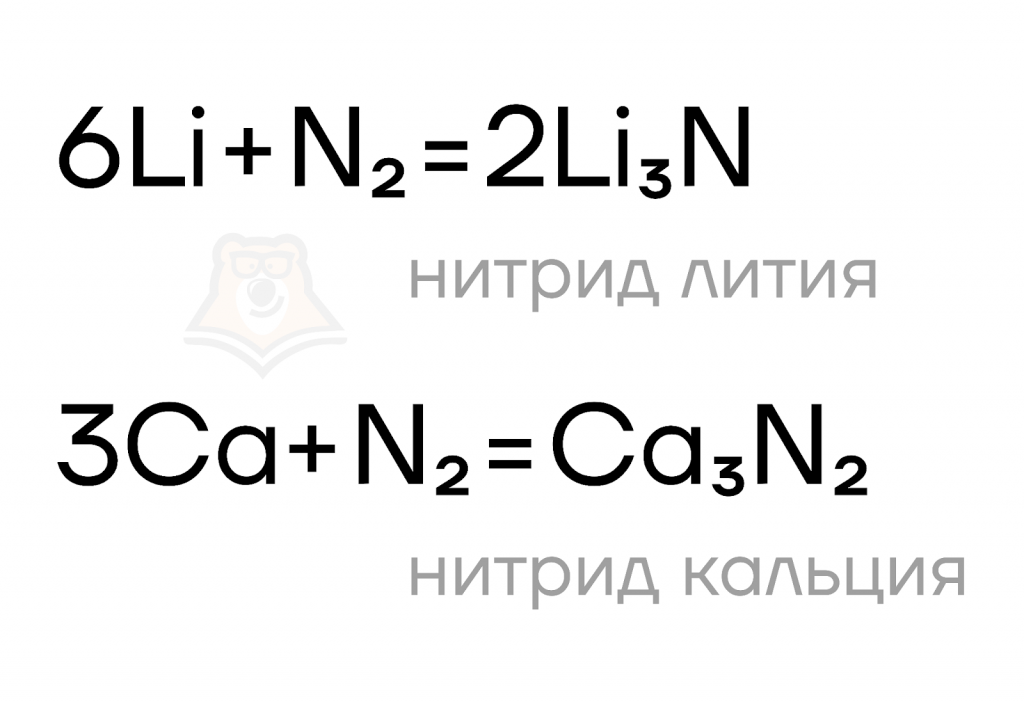
Как и многие другие бинарные соединения, нитриды могут гидролизоваться в разных средах. Уравнения этих реакций мы записываем по принципу «плюс к минусу»: к катиону присоединяем гидроксильную группу, а к аниону — водород.
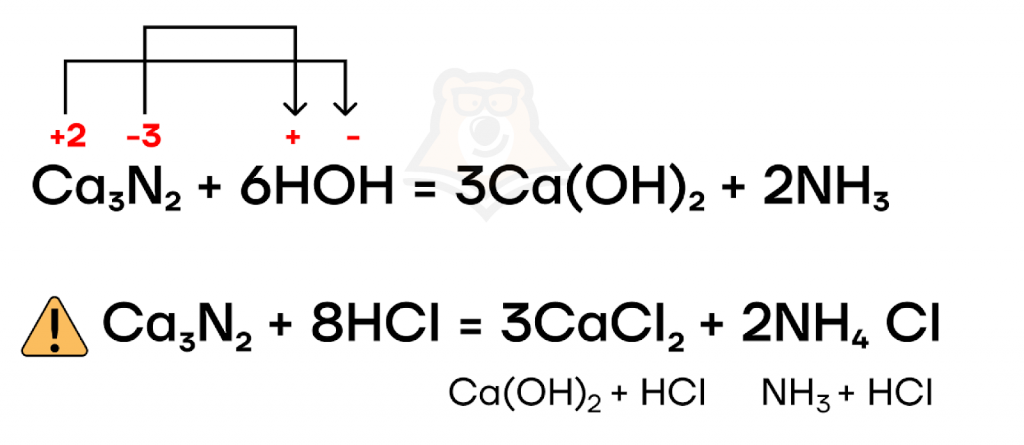
- Взаимодействие с неметаллами.
Из неметаллов азот напрямую реагирует только со фтором, кислородом и водородом, причем для проведения этих реакций нужны особые условия. С кислородом азот реагируют при электрическом разряде (или очень высокой температуре), со фтором при повышенной температуре, а реакция с водородом требует повышенной температуры давления и присутствия катализатора.

Разберем свойства одного из самых важных соединений азота — аммиака.
Аммиак
Аммиак — водородное соединение азота с химической формулой NH3. Химические свойства аммиака крайне интересны, характеризуются обилием и разнообразием реакций, в которые он может вступать, поэтому очень важно о нем поговорить.
Так как же выглядит аммиак? По физическим свойствам аммиак представляет собой хорошо растворимый в воде ядовитый газ, с резким характерным запахом нашатырного спирта.
| Нашатырный спирт — спирт или не спирт? Раствор аммиака представляет собой не просто смесь молекул воды и аммиака. Молекулы аммиака благодаря водородным связям достаточно прочно связываются с молекулами воды образуя гидрат аммиака — NH3·H2O. Гидрат аммиака — это основание, он обратимо диссоциирует с образованием гидроксид анионов. Спирты же — органические соединения, обладающие слабыми кислотными свойствами. Гидрат аммиака с точки зрения химии спиртом назвать нельзя, однако такое название прочно закрепилось в повседневной жизни. Аммиак обладает специфическим резким запахом и при вдыхании вызывает сильное раздражение нервных окончаний дыхательных путей, что позволяет использовать нашатырный спирт для выведения человека из обморочного состояния. |
- Основные свойства аммиака.
Аммиак обладает основными свойствами, поэтому реагирует со своими противоположностями — кислотами с образованием солей аммония.
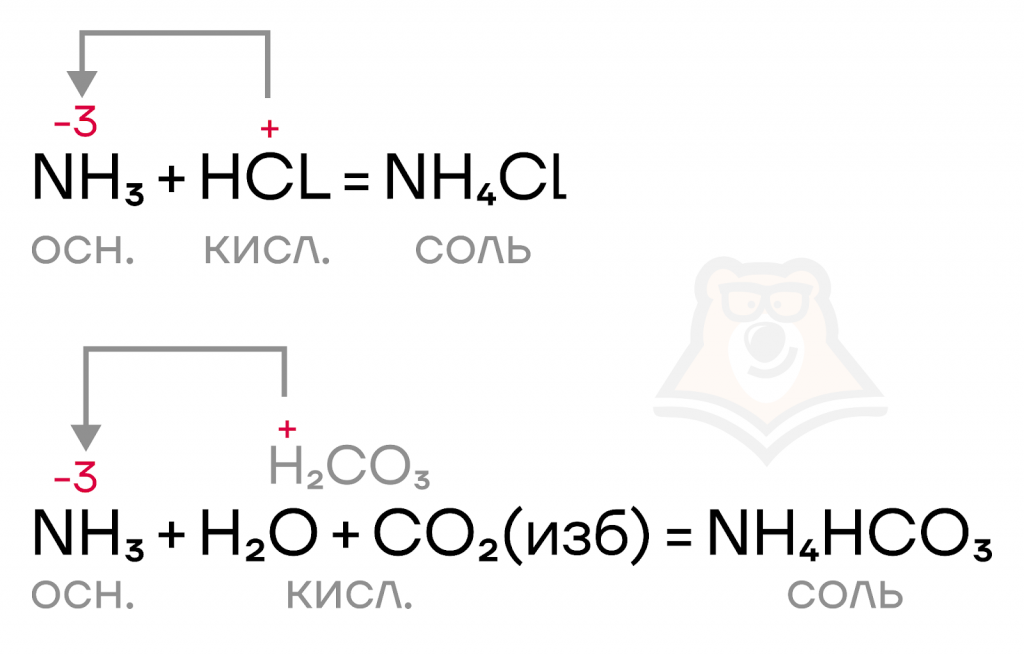
- Реакции ионного обмена с аммиаком.
Гидрат аммиака, образующийся при растворении аммиака в воде, способен к диссоциации:
NH3·H2O ⇄ NH4+ + OH—
Водный раствор аммиака вступает в реакции ионного обмена, если выполняются соответствующие условия (образование газа, осадка или слабого электролита).
3NH3·H2O + AlCl3 = Al(OH)3 + 3NH4Cl
Осадки некоторых гидроксидов получить не удается, поскольку образуются растворимые комплексные соединения. Так, например, действием раствора аммиака нельзя получить гидроксид меди(II).
Cu(OH)2 + NH3 = [Cu(NH3)4](OH)2
Аналогично в присутствии аммиака растворяется и оксид серебра(I).
Ag2O + 4NH3·H2O = 2[Ag(NH3)2]OH + 3H2O
- Аммиак как восстановитель.
За счет степени окисления -3 аммиак проявляет ярко выраженные восстановительные свойства, а значит, способен реагировать с окислителями. Например, аммиак сгорает в кислороде, в отсутствии катализатора реакция сопровождается образованием азота и воды, в присутствии катализатора возможно окисление азота до оксида азота(II) (на катализаторе происходит как бы «догорание азота» до его оксида).
В большинстве таких реакций азот, как восстановитель, повышает свою степень окисления до ближайшей устойчивой 0.

Соли аммония при нагревании разлагаются. Чаще всего в результате получается то, из чего они образуются: аммиак и соответствующая кислота, но есть и исключение — при разложении сульфата аммония образуется аммиак и гидросульфат аммония.

В составе катиона аммония содержится атом азота в степени окисления -3, способный проявлять восстановительные свойства. Если анион проявляет окислительные свойства, то при нагревании возможно протекание окислительно-восстановительной реакции.
Например, в случае бихромата и перманганата аммония, хром +6 в бихромате и марганец +7 в перманганате выступают в качестве окислителей.
В реакции с дихроматом азот повышает степень окисления с -3 до 0, а хром понижает с +6 до +3.
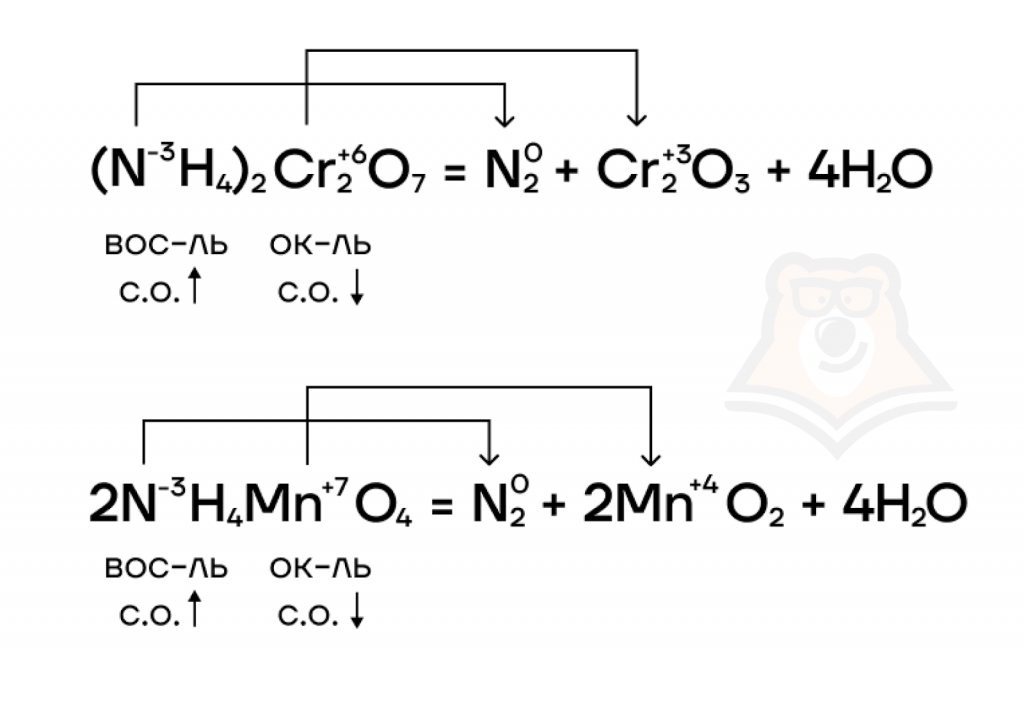
В нитрате и нитрите аммония окислителем выступают атомы азота в степени окисления +5 и +3 соответственно. В таких случаях протекает особый вид окислительно-восстановительных реакций — реакции конпропорционирования, когда из соединений, содержащих атомы азота в двух различных степенях окисления, образуется соединение, содержащее атомы этого же элемента в одной (промежуточной между исходными) степени окисления.

Получение аммиака
Мировая химическая промышленность производит огромные количества аммиака не просто так, он находит широкое применение в производстве удобрений, азотной кислоты и взрывчатых веществ.
В промышленности аммиак, в основном, получают с помощью процесса Габера — прямого синтеза аммиака из азота и водорода. А вот в лаборатории аммиак получают очень простым способом — реакцией между щелочью и солью аммония.

Синтез аммиака из простых веществ — обратимый процесс, самое время вспомнить как работает принцип Ле-Шателье, ведь эта реакция нередко встречается в задании №22 ЕГЭ.
Задание. Установите соответствие между способом воздействия на равновесную систему, в которой протекает реакция:
N2 + 3H2 ⇄ 2NH3 + Q
и направлением смещения химического равновесия при этом воздействии.
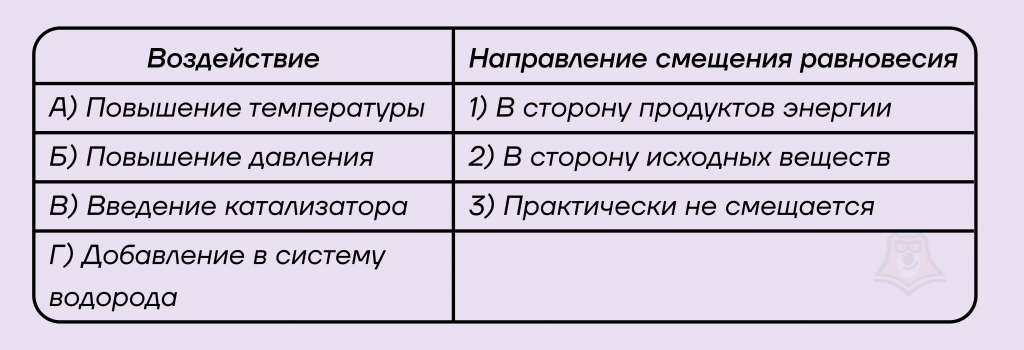
В ответ запишите выбранные номера в порядке соответствующем АБВГ.
Решение.
А. Повышение температуры приводит к смещению равновесия в направлении эндотермической реакции. Прямая реакция экзотермична, значит обратная эндотермична, равновесие смещается в сторону исходных веществ (2).
Б. Повышение давления приводит к смещению равновесия в направлении образования меньшего общего количества газов. В левой части уравнения суммарно имеем 4 моль газов, в правой — 2, равновесие смещается в сторону продуктов реакции (1).
В. Введение катализатора не влияет на положение равновесия (3).
Г. Добавление вещества в систему приводит к смещению равновесия в направлении его расходования. Водород расходуется в ходе прямой реакции — равновесие смещается в сторону продуктов реакции (1).
Ответ: 2131
Оксиды азота
Азот образует целый ряд оксидов. Давайте рассмотрим каждый из них по отдельности.
- Оксид азота(I) (веселящий газ, закись азота) — N2O
Бесцветный газ со сладковатым запахом, обладает наркотическим эффектом, может быть получен в ходе разложения нитрата аммония:
NH4NO3 = N2O + 2H2O
При нагревании разлагается:
2N2O (t) = 2N2 + O2
Не взаимодействует с кислотами и щелочами, относится к несолеобразующим оксидам.
Вступает в окислительно-восстановительные реакции, проявляет свойства как окислителя, так и восстановителя:
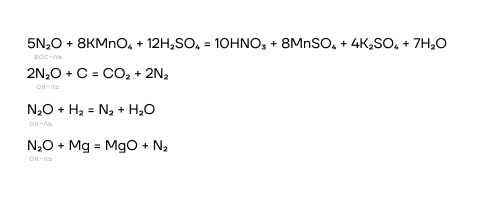
- Оксид азота(II) (окись азота) — NO
Бесцветный газ, не имеющий запаха. Может быть получен ходе в различных реакций:
1) взаимодействие азота с кислородом: N2 + O2 = 2NO;
2) каталитическое окисление аммиака: 4NH3 + 5O2 = 4NO + 6H2O;
3) взаимодействие металлов с разбавленной азотной кислотой: 3Cu + 8HNO3(разб) = 3Cu(NO3)2 +2NO + 4H2O.
Как и N2O относится к несолеобразующим оксидам, поэтому не взаимодействует с щелочами и кислотами. Выступает восстановителем:
2NO + O2 = 2NO2
10NO + 6KMnO4 + 9H2SO4 = 10HNO3 + 6MnSO4 + 3K2SO4 + 4H2O
NO + ZnO = NO2 + Zn
Также может проявлять окислительные способности:
2NO + 2SO2 = 2SO3 + N2
2NO + 2Cu = 2CuO + N2
2NO + 2H2S = 2S + N2 + 2H2O
- Оксид азота(III) — N2O3
При нормальных условиях летучая жидкость синего цвета. Может быть получен при взаимодействии оксидов азота(II) и (IV), реакция протекает при пониженных температурах:
NO + NO2 = N2O3
Кислотный оксид, при взаимодействии с водой образует азотистую кислоту, а при взаимодействии со щелочами — нитриты:
N2O3 + H2O = 2HNO2
N2O3 + 2NaOH = 2NaNO2 + H2O
При нагревании легко разлагается:
N2O3 = NO2 + NO
- Оксид азота(IV) (бурый газ, лисий хвост) — NO2
Газ бурого цвета, не имеющий запаха. Может быть получен ходе в различных реакций:
1) взаимодействие оксида азота(II) с кислородом: 2NО + O2 = 2NO;
2) разложение нитратов: 2Pb(NO3)2 = 2PbO + 4NO2 + O2;
3) взаимодействие металлов с концентрированной азотной кислотой: Cu + 4HNO3(конц) = Cu(NO3)2 + 2NO2 + 2H2O.
Относится к кислотным оксидам, образуя смесь двух кислот при взаимодействии с водой:
2NO2 + H2O = HNO3 + HNO2 (на холоде)
3NO2 + H2O = 2HNO3 + NO (при нагревании)
В присутствии кислорода образуется только азотная кислота:
4NO2 + O2 + 2H2O = 4HNO3
Аналогично реагирует с растворами щелочей, образуя соответствующие соли — нитрат и нитрит:
2NO2 + 2NaOH = NaNO3 + NaNO2 + H2O
Оксид азота(IV) проявляет сильные окислительные способности:
NO2 + SO2 + H2O = H2SO4 + NO
10NO2 + 8P = 5N2 + 4P2O5
6NO2 + 8NH3 = 7N2 + 12H2O
2NO2 + O3 = N2O5 + O2 (с кислородом реакция не протекает)
- Оксид азота(V) — N2O5
При нормальных условиях бесцветное твердое вещество, неустойчивое и летучее.
Термически разлагается: 2N2O5 = 4NO2 + O2.
Кислотный оксид:
N2O5 + H2O = 2HNO3
N2O5 + 2NaOH = 2NaNO3 + H2O
Может выступать окислителем в реакциях:
2N2O5 + 2KI = I2 + 2NO2 + 2KNO3
N2O5 + H2S = 2NO2 + S + H2O
Мы разобрали важнейшие свойства оксидов азота, а как себя ведут в химических реакциях кислоты азота?
Химические свойства азотистой кислоты HNO2
Азотистая кислота HNO2 — слабая, одноосновная, химически неустойчивая кислота, которой соответствует кислотный оксид N2O3.
- Основно-кислотное взаимодействие
Азотистая кислота проявляет кислотные свойства. Она вступает в основно-кислотные взаимодействия со своими противоположностями (основаниями и основными оксидами) с образованием солей — нитритов.

- Реакции ионного обмена

Азотистая кислота — электролит, хоть и слабый. Она чисто теоретически может вступать в реакции ионного обмена с другими электролитами: солями и основаниями.
Это вещество довольно неустойчиво, поэтому в качестве реагента в РИО ее, как правило, не используют.
- Реакции вытеснения
Как и другие кислоты-неокислители, азотистая кислота способна вступать в реакции вытеснения с металлами, стоящими до водорода в ряду активности.

- Восстановительные свойства азотистой кислоты
Азот в степени окисления +3 проявляет преимущественно восстановительные свойств, поэтому азотистая кислота вступает в реакции с типичными окислителями. Как восстановитель, он повышает степень окисления до +5:
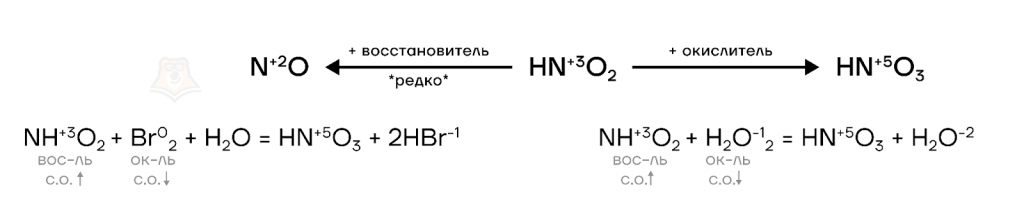
Со свойствами азотистой кислоты мы разобрались, а в какие реакции вступают ее соли — нитриты?
Соли азотистой кислоты — нитриты
Соли азотистой кислоты называют нитритами. Они преимущественно обладают восстановительными свойствами, при этом в окислительно-восстановительных реакциях образуется азотная кислота или ее соль.
Также возможны реакции, где нитриты выступают в качестве окислителей.
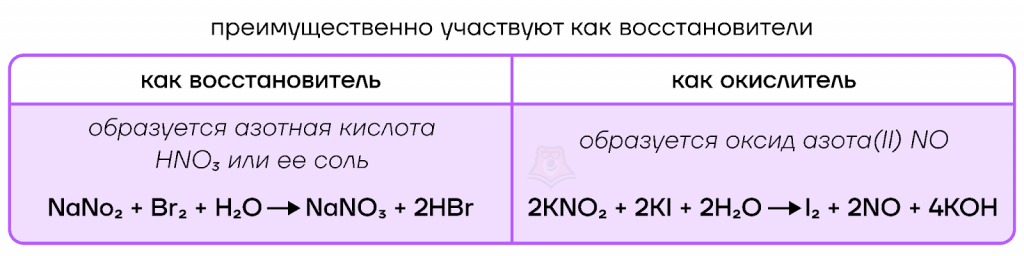
Повышаем степень окисления азота и переходим к удивительной и неповторимой азотной кислоте.
Химические свойства азотной кислоты HNO3
- Основно-кислотное взаимодействие
Азотная кислота обладает кислотными свойствами. Она способна вступать в основно-кислотные взаимодействия с веществами, которые проявляют основные свойства. В этот список входят основания, основные оксиды, амфотерные оксиды и амфотерные гидроксиды:
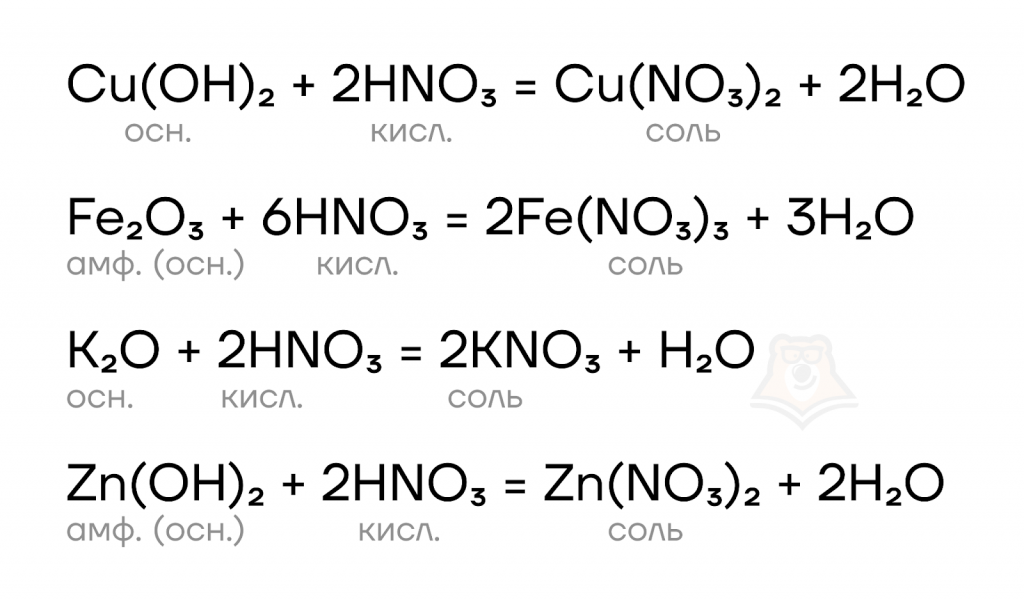
- Реакции ионного обмена
Кислоты, в том числе и азотная, являются электролитами. Поэтому они способны вступать в реакции ионного обмена с другими электролитами: солями и основаниями (если среди продуктов реакции есть газ, осадок или слабый электролит). Если хотите освежить в памяти информацию по реакциям ионного обмена — посмотрите статью «Реакции ионного обмена».
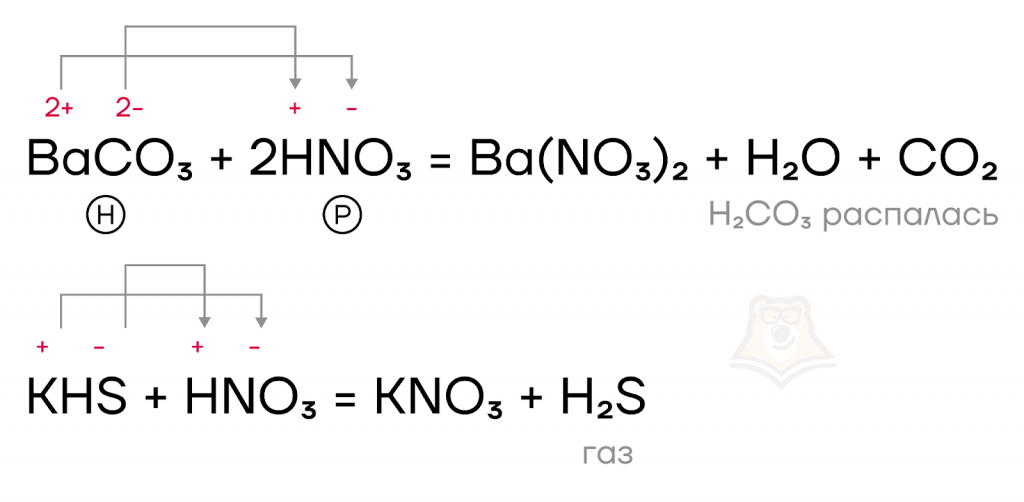
- Окислительные свойства
Азотная кислота содержит азот в степени окисления +5, из-за чего проявляется сильные окислительные свойства.
При взаимодействии с металлами продукты реакции зависят от концентрации кислоты и восстановительной способности (активности) металла. Чем меньше концентрация кислоты и выше активность металла, тем глубже (до более низкой степени окисления) протекает восстановление.
Продукты взаимодействия с азотной кислотой зависят как от активности металла, так и от концентрации кислоты. Вне зависимости от условий образуются соль и вода, а остальные продукты представлены в таблице:
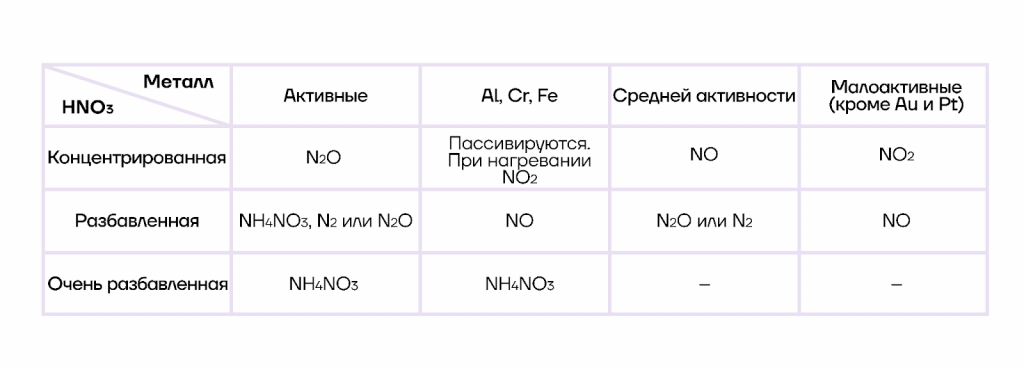
Некоторые металлы (Al, Cr, Fe) пассивируются при обычных условиях.
Пассивация металлов — переход металла в неактивное, пассивное состояние, связанный с образованием оксидной пленки.
При взаимодействии и разбавленной, и концентрированной HNO3 с металлами получается смесь продуктов, но для ЕГЭ мы пользуемся следующим упрощением:
- концентрированная азотная кислота реагирует с любыми металлами всегда до NO2;
- разбавленная азотная кислота реагирует с любыми металлами до NO;
- очень разбавленная азотная кислота реагирует с активными металлами до NH4NO3.
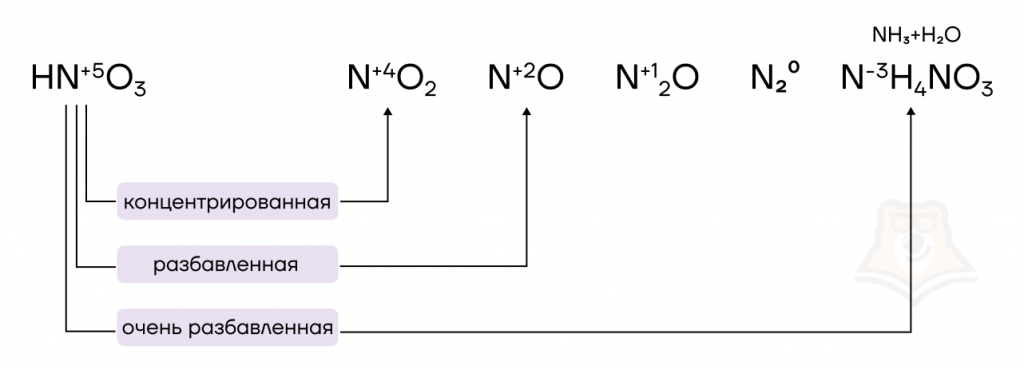

Если составители задания захотят увидеть в решении какой-то другой азотсодержащий продукт, они обязательно намекнут на это.
Например, в случае выделения N2 могут указать, что в ходе реакции «выделяется газ, преимущественно входящий в состав атмосферы», или «выделяется бескислородсодержащий газообразный продукт»
В заданиях первой части может быть так, что единственно подходящим вариантом будет ответ с нетипичным азотсодержащим продуктом, его и выбираем. В ином случае выбираем типичный продукт.
Возникает вопрос, почему может образоваться несколько соединений? В реальности реакции протекают с образованием смеси различных продуктов, но на экзамене по условиям задачи будет понятно, какое конкретно вещество необходимо писать в реакции. Если таких условий нет, то любой из указанных вариантов считается верным.

Благородные металлы (Au, Pt, Pd) не взаимодействуют с кислотами-окислителями ни при каких условиях.
Взаимодействие с металлами мы разобрали, а как реакция пойдет, если восстановителем будет неметалл? Продуктом восстановления азотной кислоты чаще всего является диоксид азота (NO2), а продукт окисления неметалла — его высшая кислородсодержащая кислота. С разбавленной кислотой реакция протекает до NO.
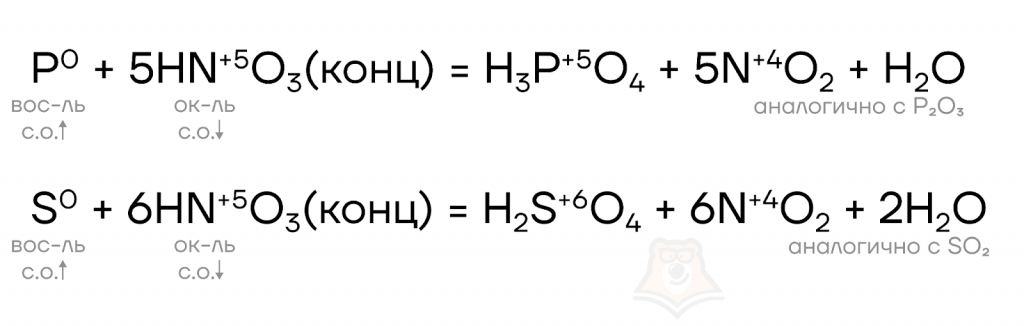
3C + 4HNO3 (разб) = 3CO2 + 4NO + 2H2O
C+ 4HNO3 (конц) = CO2 + 4NO2 + 2H2O
S + 2HNO3 (разб) = H2SO4 + 2NO
I2 + 10HNO3 = 2HIO3 + 10NO2 + 4H2O
В случае сложных веществ продукты реакции опять-таки зависят от восстановительной способности восстановителя и концентрации кислоты.
Ниже представлены примеры некоторых окислительно-восстановительных реакций с участием азотной кислоты.
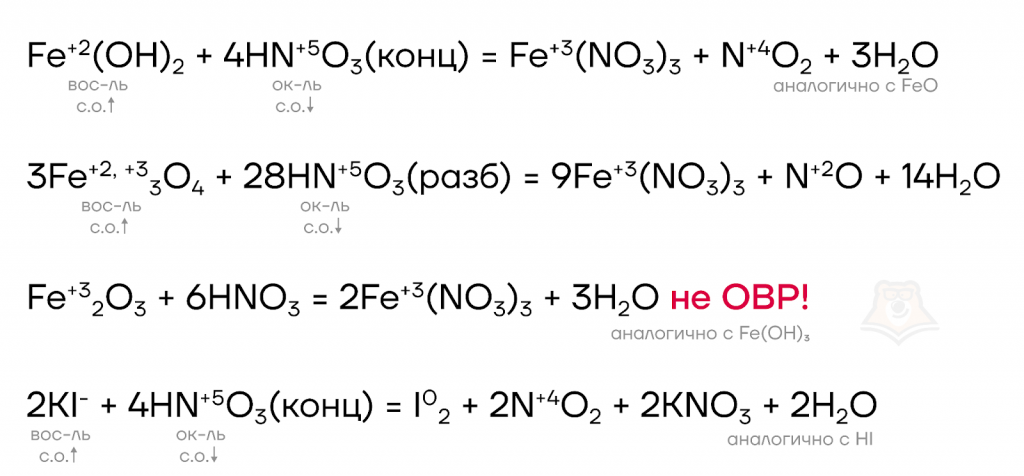
Азотная кислота обладает удивительными свойствами, но ее соли (нитраты) также достойны внимания.
Соли азотной кислоты — нитраты
Нитраты — это соли азотной кислоты, которые обладают всеми свойствами обычных солей.
- Реакции ионного обмена
Соли могут распадаться на ионы, потому что они являются электролитами. Они способны вступать в реакции ионного обмена с другими электролитами: солями, основаниями и кислотами (если исходные вещества растворимы, а среди продуктов есть газ, осадок или слабый электролит).

- Термическое разложение нитратов
Разложение нитратов может протекать по нескольким схемам. Это напрямую зависит от активности металла в составе соли:
- нитраты металлов до Mg (кроме Li): нитрит металла и кислород (MeNO2 + O2);
- нитраты металлов от Mg до Cu (и Li): оксид металла, диоксид азота и кислород (MeO + NO2 + O2);
- нитраты металлов после Cu: металл, диоксид азота и кислород (Me, NO2, O2).


Обратите внимание!
- Нитрат лития разлагается так же, как и нитраты большинства металлов, а не как нитрат активного металла:
4LiNO3 = 2Li2O + 4NO2 + O2
- Нитраты железа(II), хрома(II) и марганца(II) вступают при разложении в более сложные ОВР, где они сами также являются восстановителями:
4Fe(NO3)2 = 2Fe2O3 + 8NO2 + O2
4Cr(NO3)2 = 2Cr2O3 + 8NO2 + O2
Mn(NO3)2 = MnO2 + 2NO2
С реакциями разложения солей нужно быть внимательными, особенно в вопросах про классификацию реакций. Посмотрим, где нас хотят поймать на особенностях химии азота в задании №17 ЕГЭ.
Задание. Из предложенного перечня выберите все окислительно-восстановительные реакции.
1. Термическое разложение карбоната аммония.
2. Термическое разложение бихромата аммония.
3. Термическое разложение нитрата натрия.
4. Термическое разложение нитрита аммония.
5. Термическое разложение хлорида аммония.
Решение:
1.(N-3H4)2CO3 = N-3H3 + CO2 + H2O — Не ОВР
2.(N-3H4)2Cr+62O7 = N02 + Cr+32O3 + 4H2O — ОВР
3.2NaN+5O-23 = 2NaN+3O2 + O02 — ОВР
4.N-3H4N+3O2 = N02 + 2H2O — ОВР
5.N-3H4Cl = N-3H3 + HCl — Не ОВР
Ответ: 245
На этом разговор о химии азота подходит к концу, мы осветили важные моменты, касающиеся азота как элемента и простого вещества, а также не обошли стороной и его наиболее важные соединения — аммиак, оксиды азота и азотную кислоту. Далее советуем познакомиться со свойствами соседа азота по группе — фосфора, сделать это можно в статье «Элементы VА группы. Фосфор».
Термины
Бинарные соединения — соединения состоящие из атомов двух элементов.
Катализатор — вещество увеличивающее скорость химической реакции, но не расходующееся по мере ее протекания.
Электронная конфигурация — распределение электронов по атомным орбиталям атома.
Фактчек
- Азот — химический элемент VА группы, который входит в категорию пниктогенов.
- Высшая степень окисления азота +5, но высшая валентность — только IV.
- Азот как простое вещество химически инертен и вступает в реакции только с очень активными веществами (активные металлы, фтор, кислород).
- Азот образует множество соединений: оксиды, азотную кислоту, соли, нитриды, аммиак.
- Аммиак является типичным восстановителем за счет низшей степени окисления азота -3.
- Азот образует 5 оксидов за счет большого разнообразия степеней окисления.
- Азотная кислота — сильная кислота, которая может проявлять окислительные свойства из-за азота в степени окисления +5.
- При реакции с металлами важна концентрация азотной кислоты — в зависимости от нее будут выделяться разные продукты.
- Нитраты легко разлагаются в зависимости от входящего в них катиона металла.
Проверь себя
Задание 1.
Какова конфигурация внешнего электронного слоя атома азота в основном состоянии?
- 2s22p3
- 2s22p2
- 3s23p3
- 3s23p2
Задание 2.
Какова максимально возможная валентность у атома азота?
- III
- IV
- V
- VI
Задание 3.
У какого оксида азота есть тривиальное название «веселящий газ»?
- N2O
- NO
- NO2
- N2O5
Задание 4.
Какой металл не будет реагировать с концентрированной азотной кислотой при комнатной температуре?
- Медь
- Свинец
- Кадмий
- Алюминий
Задание 5.
Нитрат какого металла разлагается на соответствующий оксид металла, оксид азота(IV) и кислород?
- Барий
- Ртуть
- Литий
- Натрий
Ответы: 1. — 1 ; 2. — 2; 3. — 1; 4. — 4; 5. — 3.

 к списку статей
к списку статей