
На этой странице вы узнаете
- Как активированный уголь может помочь нам в быту?
- Обычный чай — это химический индикатор?
- Как фиалки открыли лакмус?
Если бы вы сейчас смотрели видео-канал, а не читали статью, мы бы показали вам один из самых интересных опытов под названием «Фараонова змея» или «борода Фараона». Он действительно очень зрелищный — будто бы из синего пламени выползают и вьются коричневые змеи. Поищите в сети, если заинтересовались.
Для многих самое интересное в химии — эксперименты. Очень интересно смешивать вещества и наблюдать различные признаки реакции. Но проведение лабораторных экспериментов — это еще и своего рода исследование, для успешного проведения которого нужно знать основные методы исследования и уметь работать с оборудованием.
Научные методы исследования химических веществ и превращений
Помните молодого химика из нашей статьи «Правила работы в лаборатории. Лабораторная посуда и оборудование»? Так вот, после покупки всего необходимого для своей лаборатории он начал покорять химию, но столкнулся с вопросом: а как вообще исследуют химические вещества и их превращения? Давайте поможем нашему молодому специалисту.
Есть несколько методов химического исследования:
- Наблюдение.
Наблюдение в науке несколько отличается от наблюдения в привычном нам смысле. Мы должны точно определить, что именно собираемся наблюдать, составить план, сформулировать гипотезу о том, что мы должны увидеть. Например, наблюдать мы можем за признаками реакций — изменение цвета раствора, растворение или выпадение осадка, выделение газа.
- Эксперимент.
Эксперимент — это проведение химической реакции в полностью контролируемых и управляемых нами условиях. С помощью эксперимента мы подтверждаем или опровергаем какую-либо гипотезу.
- Моделирование.
Иногда эксперимент невозможно провести в соответствующих условиях. Например, наш химик собрался проводить реакции с выделением токсичных паров ртути, как в ныне запрещенном опыте с «Фараоновой змеей». Но вытяжным шкафом еще пока не обзавелся.
В таком случае эксперимент проводится с помощью моделирования. Оно может быть предметным — модели атомов, элементов, веществ, химических установок и знаковым — символы химических элементов, формулы веществ, уравнения реакций. Когда мы с вами решаем химическую задачу, можно сказать, мы применяем метод моделирования.
Методы разделения смесей и очистки веществ
Наш молодой химик столкнулся с тем, что далеко не все вещества в жизни находятся в чистом виде. Для получения чистых веществ существуют следующие способы разделения смесей и очистки веществ:
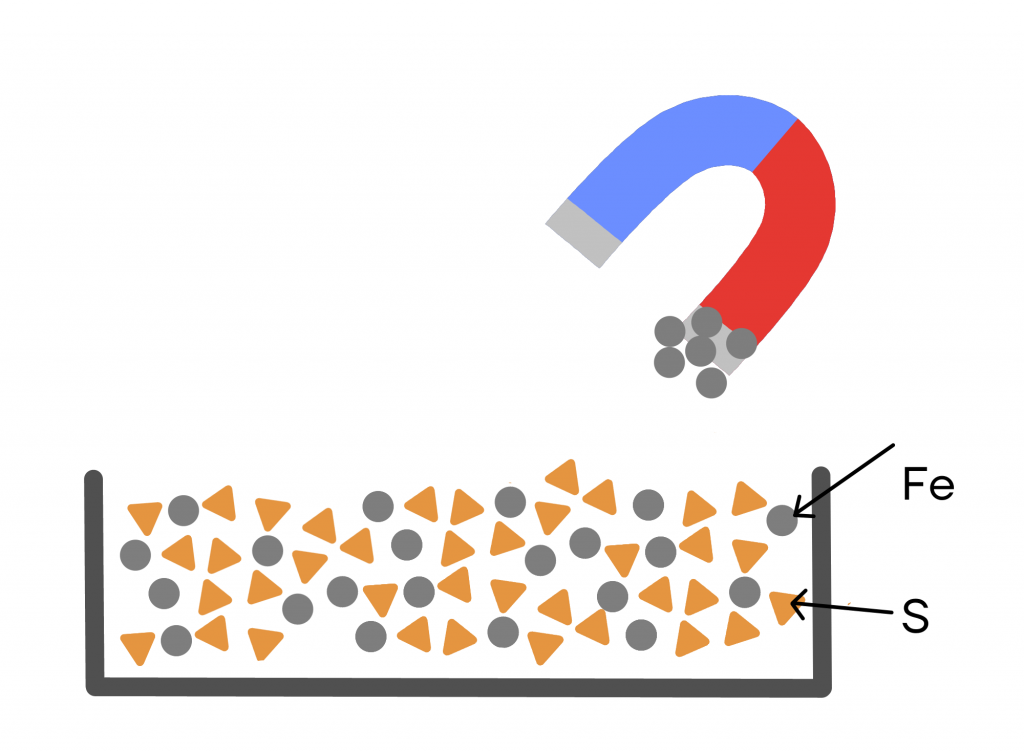
- Использование магнита. Здесь все легко. Если смесь содержит железо, кобальт или никель, то магнит их притягивает к себе.
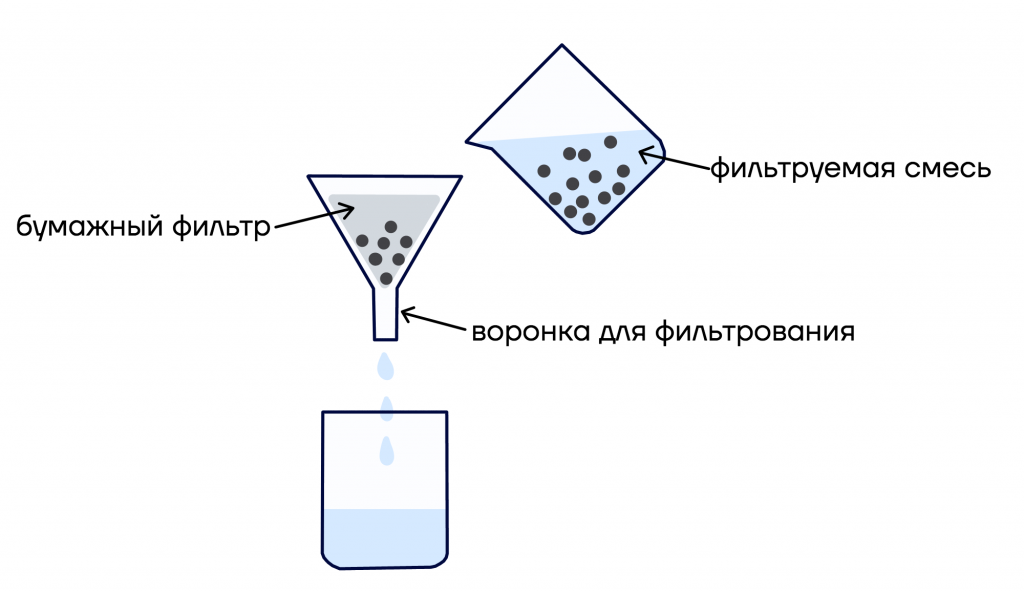
- Воронка фильтрования. Чаще всего нужна для разделения воды и нерастворимых в ней твердых веществ.
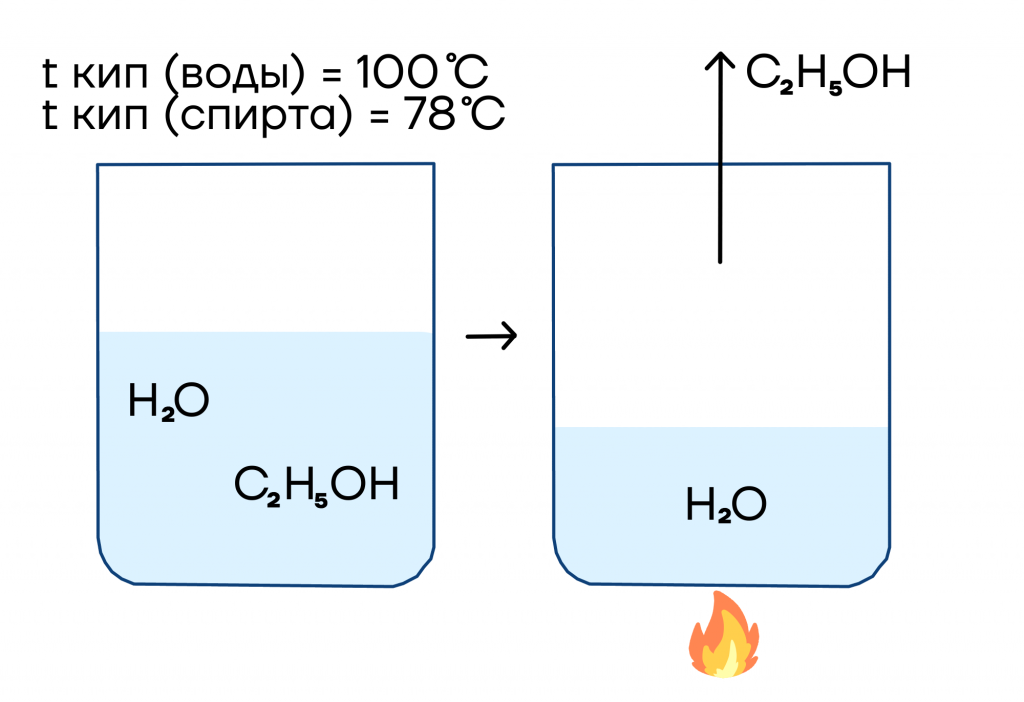
- Выпаривание. Когда происходит образование пара? При нагревании какого-то раствора. Если есть растворитель (чаще всего вода) и какое-то растворенное в нем вещество, то этот метод нам подходит. Температуры кипения воды и растворенного вещества должны быть различными.
- Делительная воронка. С ее помощью мы разделяем несмешивающиеся друг с другом жидкости, то есть жидкости с разной плотностью.
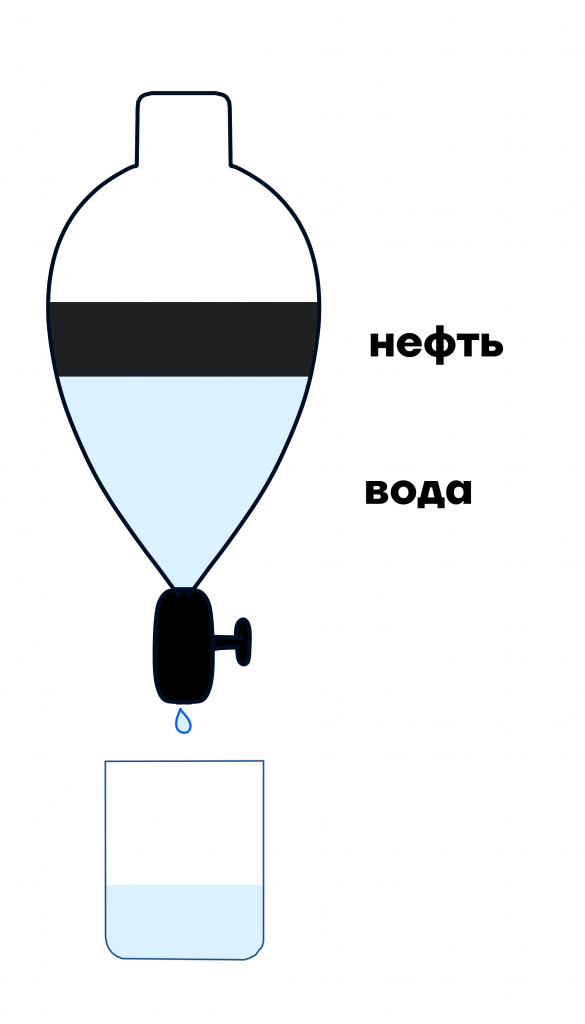
Например:
- бензин и воду;
- масло и воду.
Жидкость с меньшей плотностью «всплывет». Например, вспомните, как в холодном супе капельки жира или масла всегда всплывают наверх, так происходит, потому что плотность жира меньше плотности воды.
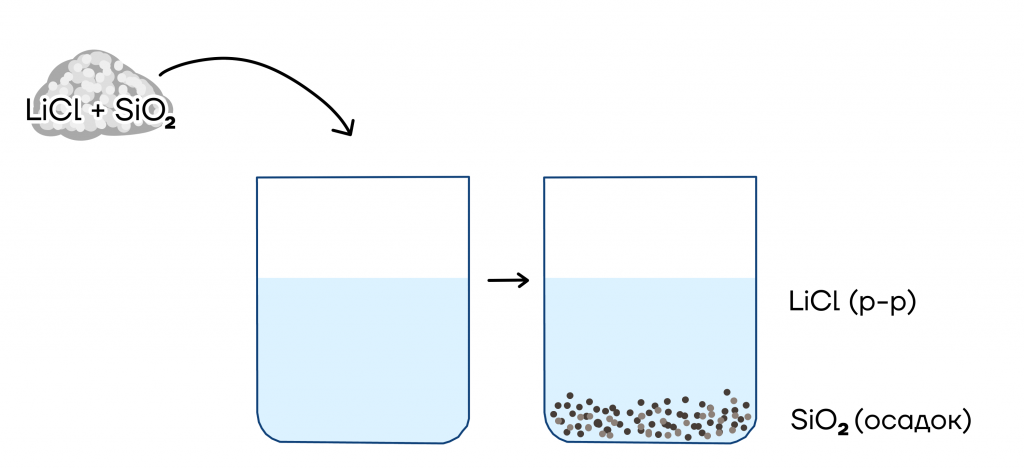
- Обработка водой. Таким способом разделяют два твердых вещества, одно из которых растворимо в воде, а другое — нет.
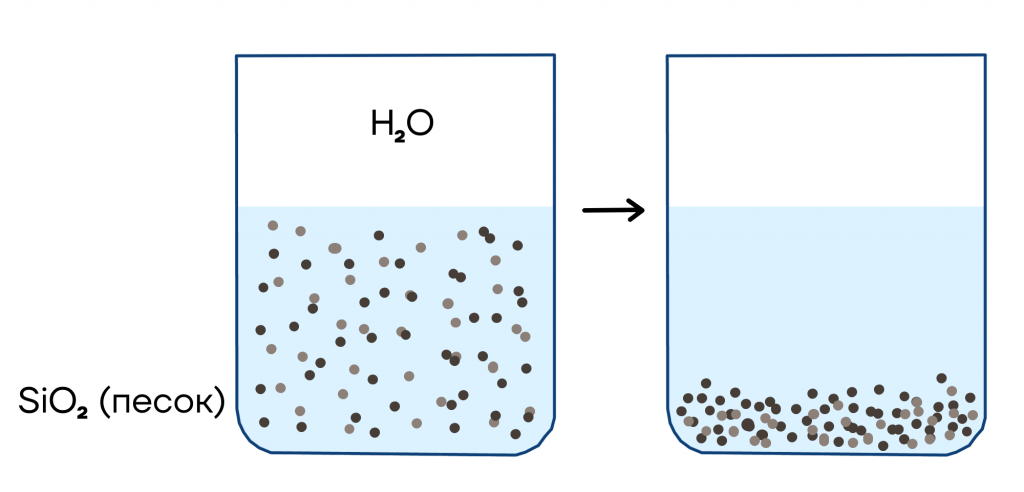
- Отстаивание. Таким способом разделяем почти любую гетерогенную смесь. Здесь даже делать ничего не надо. Просто ждем, пока твердое вещество осядет на дно.
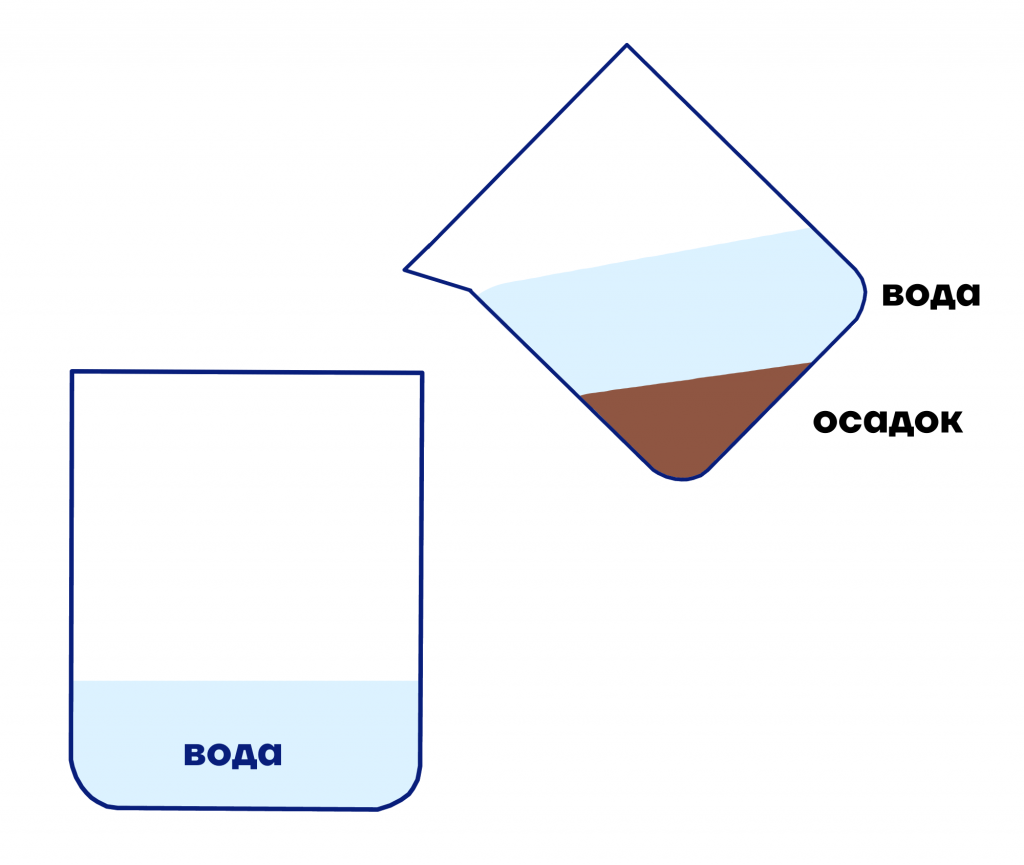
- Декантация. Этот метод используют для разделения раствора и осадка — например, воды и сульфата бария — нерастворимой соли. Просто сливаем жидкость.
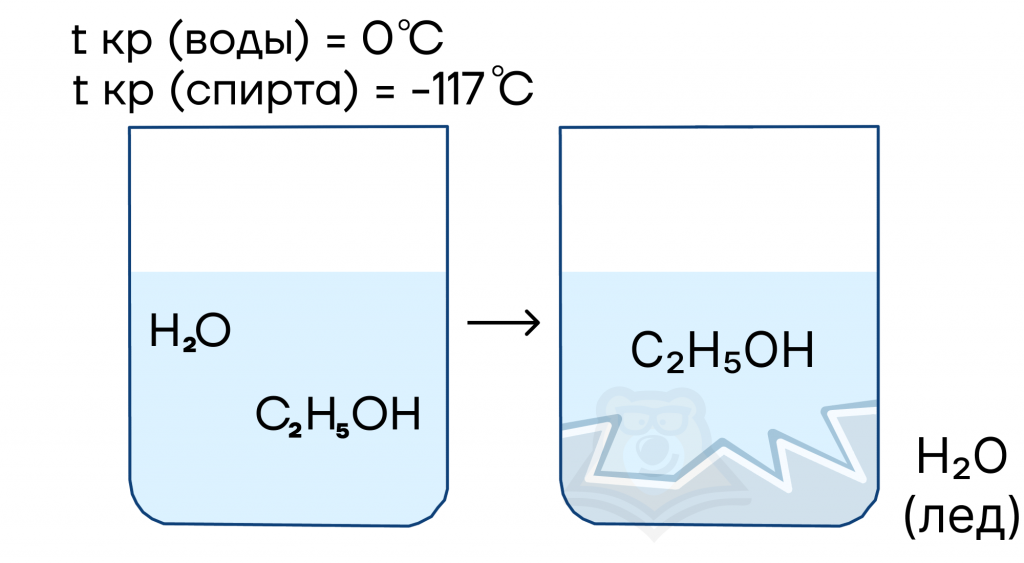
- Кристаллизация («метод снеговика»). Для разделения смеси жидкостей с разными температурами замерзания, смесь можно заморозить до меньшей температуры замерзания одного из веществ, и тогда оно замерзнет, а второе останется жидким.
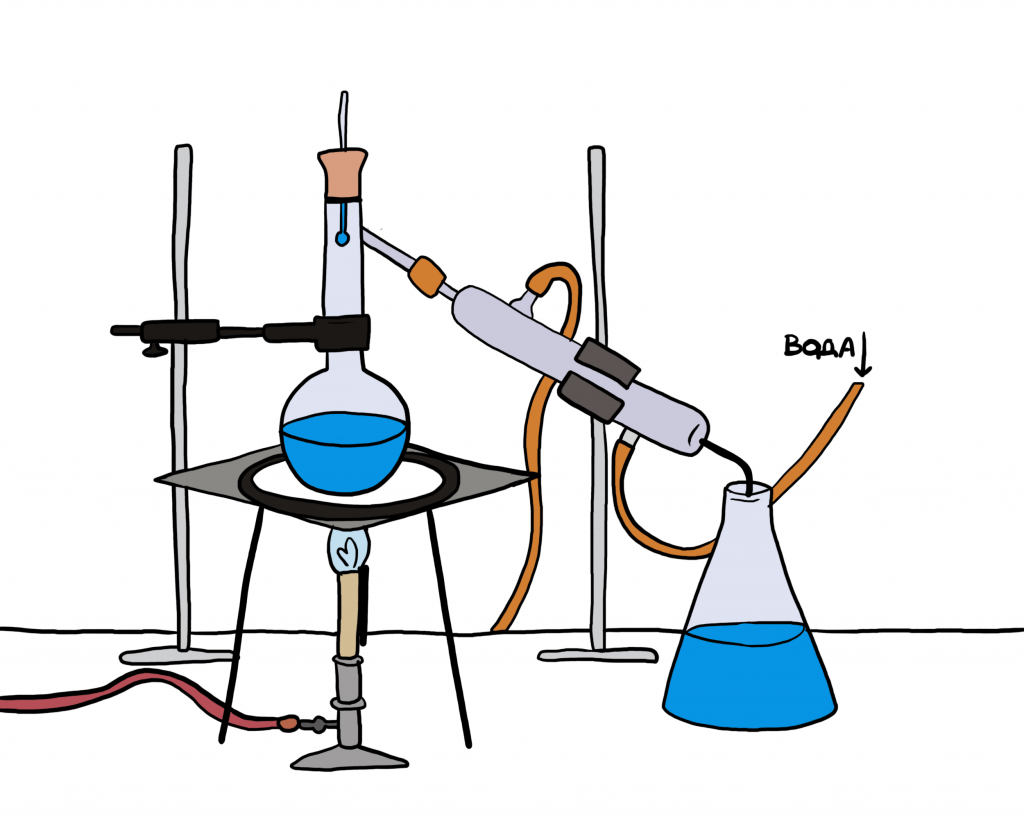
- Фракционная перегонка. Таким способом разделяем две растворимые друг в друге жидкости с разными температурами кипения.
Примеры:
- ацетон и вода;
- спирт и вода;
- гексан и бензол.
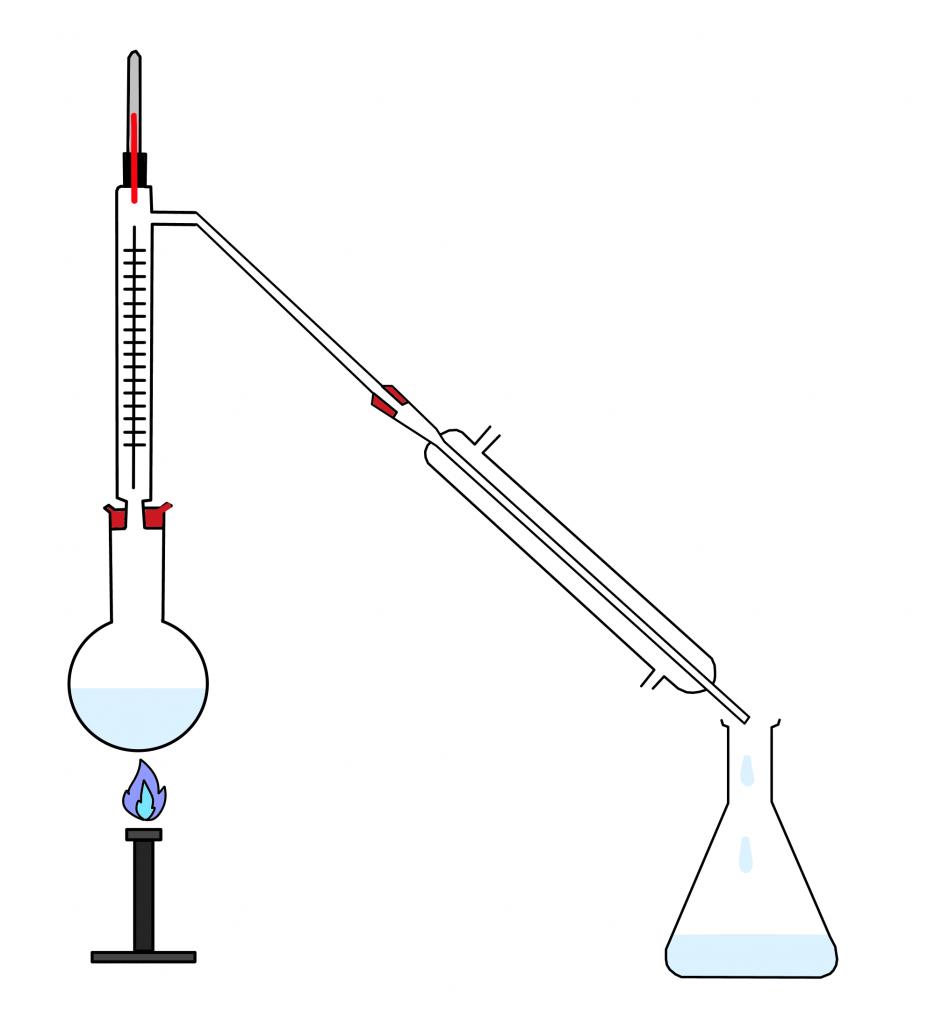
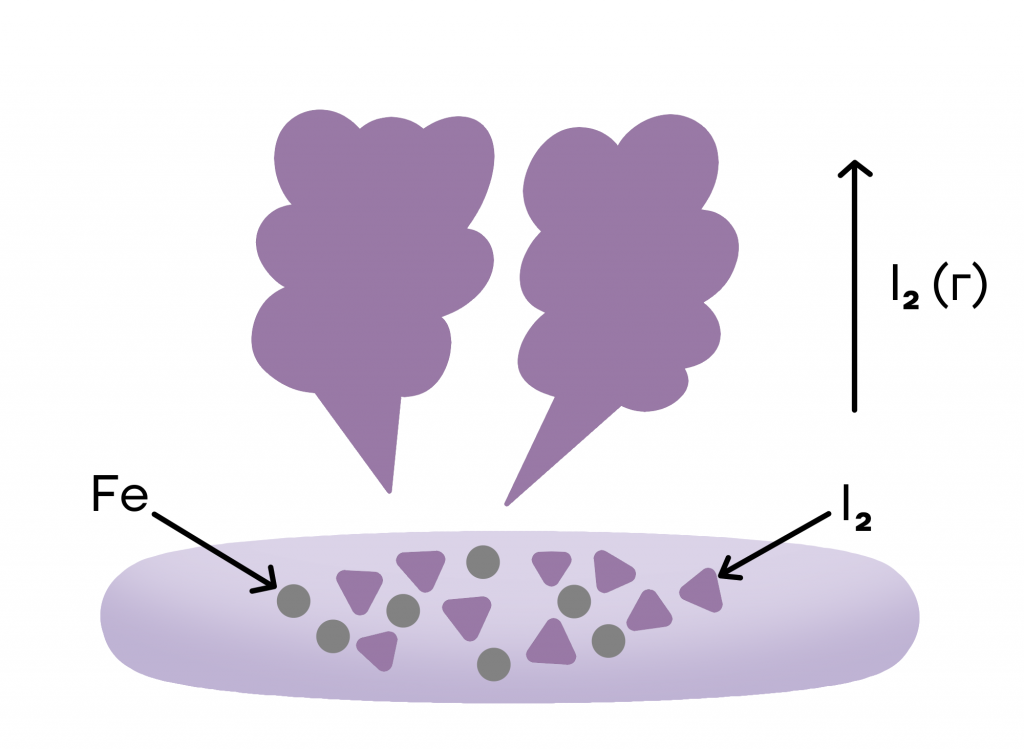
- Возгонка. Йод и некоторые другие вещества способны возгоняться (сублимироваться), то есть переходить из твердого агрегатного состояния сразу в газообразное, минуя фазу жидкости. Например, так очищают йод от железных опилок. Как они оказались вместе это уже другой вопрос.
- Адсорбция. Для очистки газов и жидкостей часто используют метод адсорбции. В процессе адсорбируемое вещество накапливается на поверхности другого. К адсорбентам относятся активированный уголь и силикагель.
| Как активированный уголь может помочь нам в быту? Активированный уголь хорошо знаком нам как средство при пищевых отравлениях. Он, словно губка, впитывает в себя все токсичные вещества из нашего организма. Также он используется в фильтрах для очистки воздуха и воды. А еще активированный уголь можно использовать как средство для избавления от неприятных запахов — просто поставьте миску с несколькими таблетками угля рядом с мусорным ведром, кошачьим туалетом или корзиной для грязного белья. Хорошо активированный уголь помогает комнатным растениям, если в земле завелась плесень. Добавьте измельченный активированный уголь в почву, он будет впитывать лишнюю влагу и препятствовать развитию плесени. |
Индикаторы
Еще есть такие товарищи, которых зовут индикаторы. Это соединения, позволяющие визуализировать изменение концентрации какого-либо вещества в растворе. Их трое:
- лакмус,
- метилоранж,
- фенолфталеин.
| Обычный чай — это химический индикатор? А вы когда-нибудь задумывались, почему чай светлеет, когда мы кладем туда кусочек лимона? Дело в том, что в листьях черного чая содержится пигмент теарубигин, который в кислой среде (добавление дольки лимона) светлеет, а в щелочной — наоборот, темнеет. Вы можете это проверить, добавив в чай кальцинированной соды (Na2CO3) и создав тем самым щелочную среду. Пить такой чай с кальцинированной содой, конечно, нельзя. Получается, чай — это химический индикатор? Можно сказать, что да. Так что наш молодой химик в экстренных ситуациях при отсутствии других классических индикаторов может заварить чайный пакетик. |
Для чего они нужны?
Для определения среды раствора. Подробнее про среды раствора можно прочитать в статье «Гидролиз солей».
Цвет каждого индикатора в конкретной среде отражен в таблице:
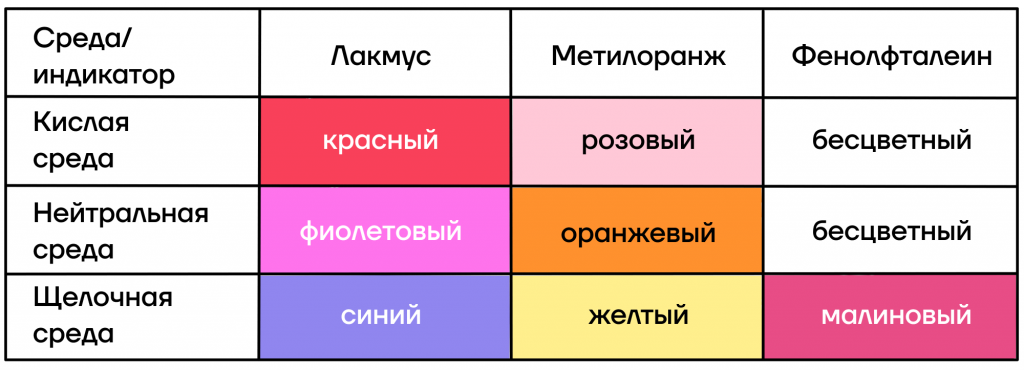
Если запомнить цвета индикаторов для вас трудно, молодой химик сочинил (он еще немного и поэт) вот такие стишки:
Лакмус
Индикатор лакмус красный
кислоту укажет ясно.
Индикатор лакмус синий,
щелочь здесь, не будь разиней.
Когда ж нейтральная среда,
он фиолетовый всегда.
Метилоранж
От щелочи я желт как в лихорадке,
Я розовею от кислот, как от стыда.
И я бросаюсь в воду без оглядки,
Здесь я оранжевый практически всегда.
Фенолфталеин
Фенолфталеиновый — в щелочах малиновый,
Но несмотря на это в кислотах он без цвета.
- Окраску лакмуса еще можно запомнить по кодовому слову KFC — красный, фиолетовый, синий.
- Первые буквы названий цветов окраски метилоранжа — розовый, оранжевый, желтый — сливаются в слово «РОЖь».
- А с фенолфталеином еще проще — просто запомнить, что он окрасится только в щелочной среде.
| Как фиалки открыли лакмус? Такое понятие, как химические индикаторы открыл известный химик Роберт Бойль. А было это так: в лабораторию Бойля зашел садовник и принес ему корзину фиалок. Но в это время Бойлю нужно было проводить опыт, поэтому фиалки он машинально бросил на стол. В ходе опыта выделялся едкий дым, и после его завершения Бойль увидел, что фиалки дымились. Чтобы спасти цветы, Бойль поставил их воду и увидел, что их лепестки поменяли цвет с фиолетового на красный. Бойль не прошел мимо такого явления, а принялся готовить растворы с разными средами и опускал туда фиалки, которые в некоторых растворах меняли цвет лепестков. Затем он начал проводить такие же эксперименты с другими растениями и определил, что лучшие результаты дает лакмусовый лишайник. Позднее он придумал пропитать отваром этого лишайника бумажные полоски, высушить их и использовать как индикаторы. Именно эти индикаторы помогли Бойлю открыть фосфорную кислоту, полученную при сжигании фосфора. |
Вот мы вместе с нашим молодым ученым и разобрали основные принципы работы в химической лаборатории. А теперь пришло время проводить всевозможные реакции и делать научные открытия!
Фактчек
- При исследовании химических веществ и их превращений используют наблюдение, эксперимент и моделирование.
- Наблюдение (смотрим на признаки реакции — изменение цвета, растворение или выпадение осадка, выделение газа).
- Эксперимент (своими руками проводим реакции, смешиваем реагенты).
- Моделирование (создаем модель, то есть аналог вещества).
- Есть много способов разделения веществ, но их легко запомнить с помощью логики и ассоциаций.
Проверь себя
Задание 1.
Что разделяют отстаиванием?
- песок и воду
- два неметалла
- гомогенную смесь
Задание 2.
Что разделяют магнитом?
- воду и бензин
- железо и серу
- хлор и бром
Задание 3.
Какого цвета фенолфталеин в щелочах?
- малиновый
- желтый
- красный
- белый
Задание 4.
Кислую среду нельзя отличить от нейтральной с помощью…
- лакмуса
- метилоранжа
- фенолфталеина
Задание 5.
В качестве химического индикатора можно использовать…
- раствор пищевой соды
- чай
- апельсиновый сок
Ответы: 1. — 1; 2. — 2; 3. — 1; 4. — 3; 5. — 2.

 к списку статей
к списку статей 



